Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Gọi số mol H2 phản ứng là a (mol)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
mgiảm = mO(mất đi) = 4,8 (g)
=> nO(mất đi) = \(\dfrac{4,8}{16}=0,3\left(mol\right)\)
=> \(n_{H_2O}=0,3\left(mol\right)\)
=> \(n_{H_2}=0,3\left(mol\right)\)
=> \(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b) \(n_{Fe}=0,2\left(mol\right)\)
=> \(m_{Fe}=0,2.56=11,2\left(g\right)\)
\(n_{Fe_2O_3}=0,1\left(mol\right)\)
=> \(m_{Fe_2O_3}=0,1.160=16\left(g\right)\)

a) Gọi số mol Fe2O3 là a (mol)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
a---->3a--------->2a
=> 160a - 56.2a = 9,6
=> a = 0,2 (mol)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
b) m = 0,2.160 = 32 (g)
mFe = 0,4.56 = 22,4 (g)

\(a,\\ Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\\ Fe_3O_4+4H_2\rightarrow\left(t^o\right)3Fe+4H_2O\)
Loại phản ứng: Phản ứng thế
\(b,n_{Fe}=2.n_{Fe_2O_3}+3.n_{Fe_3O_4}=2.\dfrac{32}{160}+3.0,15=0,85\left(mol\right)\\ m_{Fe}=0,85.56=47,6\left(g\right)\\ c,n_{H_2}=\dfrac{32}{160}.3+4.0,15=1,2\left(mol\right)\\ V_{H_2\left(đktc\right)}=1,2.22,4=28\left(l\right)\)
Em xem sao oxit sắt lại hỏi KL nhôm nha! Vô lí!!!

a)\(n_{Al}=\dfrac{18}{27}=\dfrac{2}{3}mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{2}{3}\) 1
\(V_{H_2}=1\cdot22,4=22,4l\)
b)\(n_{Fe_2O_3}=\dfrac{32}{160}=0,2mol\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,2 1 0,4 0,6
\(m_{Fe}=0,4\cdot56=22,4g\)
c)\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,4 \(\dfrac{4}{15}\)
\(V_{O_2}=\dfrac{4}{16}\cdot22,4=\dfrac{448}{75}l\)
\(V_{kk}=5V_{O_2}=\dfrac{448}{15}l\approx29,87l\)

a)\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,3 0,3 0,3
\(V_{H_2}=0,3\cdot22,4=6,67l\)
\(m_{FeCl_3}=0,3\cdot127=38,1g\)
b)\(n_{Fe_2O_3}=\dfrac{18}{160}=0,1125mol\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,1125 0,3 0 0
0,1 0,3 0,2 0,3
0,0125 0 0,2 0,3
\(m_{Fe}=0,2\cdot56=11,2g\)

FeO + CO -> Fe + CO2
mol: x -> x
pt2: Fe2O3 + CO ->2 Fe + CO2
mol: y -> 2y
theo gt thu được 2.94 g
Fe trong đó có Fe tạo thành và Fe ban đầu và gọi Z là số mol Fe ban đầu
=> ta có Pt : 72x + 160y +56z=3.54 (1)
và x + 2y + z =3.92/56=0.0525 (2)
hh trên vào CuSO4 thì chỉ có Fe phản ứng
pt: Fe + CuSO4 -> FeSO4 + Cu
mol: z -> z
thu được 3.72g rắn gồm Cu , FeO, Fe2O3
=> ta có pt: 72x + 160y + 64Z=3.72 (3)
từ (1),(2),(3) ta có x=0.015= nFeO , y=0.0075 mol =nFe2O3 , z=0.0225 mol=nFe
Có số mol áp dụng công thức m=n*M em tự tính khối lượng các chất nha
Số ko đẹp lắm nên số mol hơi dài,cứ giữ nguyên để tính để tránh sai số
CHÚC EM HỌC TỐT !!!!!!(nhớ hậu tạ nha hi hi.....)

PTHH : \(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
.............0,05........0,2.......0,15.........
Có : \(\left\{{}\begin{matrix}n_{H_2}=0,2\left(mol\right)\\n_{Fe_3O_4}=0,075\left(mol\right)\end{matrix}\right.\)
- Theo phương pháp ba dòng .
=> Sau phản ứng H2 hết, Fe3O4 còn dư ( dư 0,025 mol )
=> \(m=m_{Fe3o4du}+m_{Fe}=14,2\left(g\right)\)
b, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
...0,15.....0,3.........0,15..............
\(Fe_3O_4+8HCl\rightarrow2FeCl_3+FeCl_2+4H_2O\)
.0,025......0,2..........0,05.........0,025...................
Có : \(V=\dfrac{n}{C_M}=\dfrac{n}{1}=n_{HCl}=0,2+0,3=0,5\left(l\right)\)
Lại có : \(m_M=m_{FeCl2}+m_{FeCl3}=30,35\left(g\right)\)

a. áp dụng định luật bảo toàn nguyên tố
=> 4,8 g là khối lượng O trong oxit sắt
=> nO = 0,3 ; nFe = 0,2
CT oxit sắt là Fe2O3
b. Fe2O3 + 3CO ---> 2Fe + 3CO2
nCO = 0,3 mol
dùng dư 10% => nCO = 0,3 x 110% = 0,33 mol
CÂU C BN TỰ LM NHA, LƯỜI WÁ![]()
Gọi công thức oxit sắt:Fex0y.
Fex0y+yCO=>xFe+yC02
0.2/x------------>0.2(mol)
_Sau pư khối lượng chất rắn giảm 4.8 g so với ban đầu:
=>mFe=16-4.8=11.2(g)
=>nFe=11.2/56=0.2(mol)
=>n(Fex0y)=0.2/x(mol)
Mà nFex0y=16/(56x+16y) (mol)
=>16x=0.2(56x+16y)
<=>4.8x=3.2y
<=>x/y=2/3
Vậy công thức oxit sắt là Fe203.
_Khí sinh ra là C02 cho tác dụng với dd NaOH:
nC02=0.2*3=0.6(mol)
_Khối lượng dd tăng cũng chính là khối lượng C02 tham gia:
C02+2NaOH=>Na2S03+H20
0.6--->1.2-------->0.6(mol)
=>mC02=0.6*44=26.4(g)
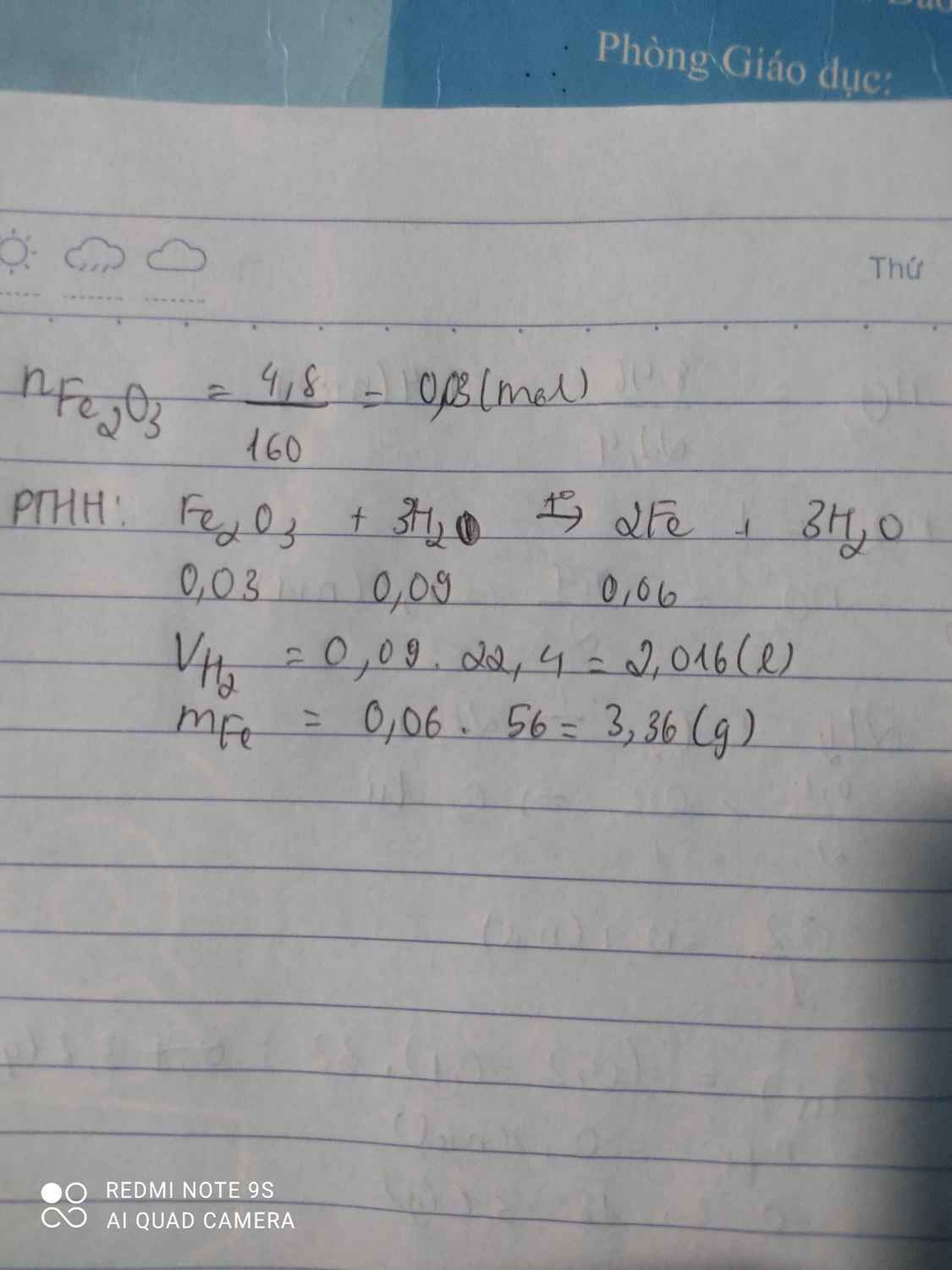
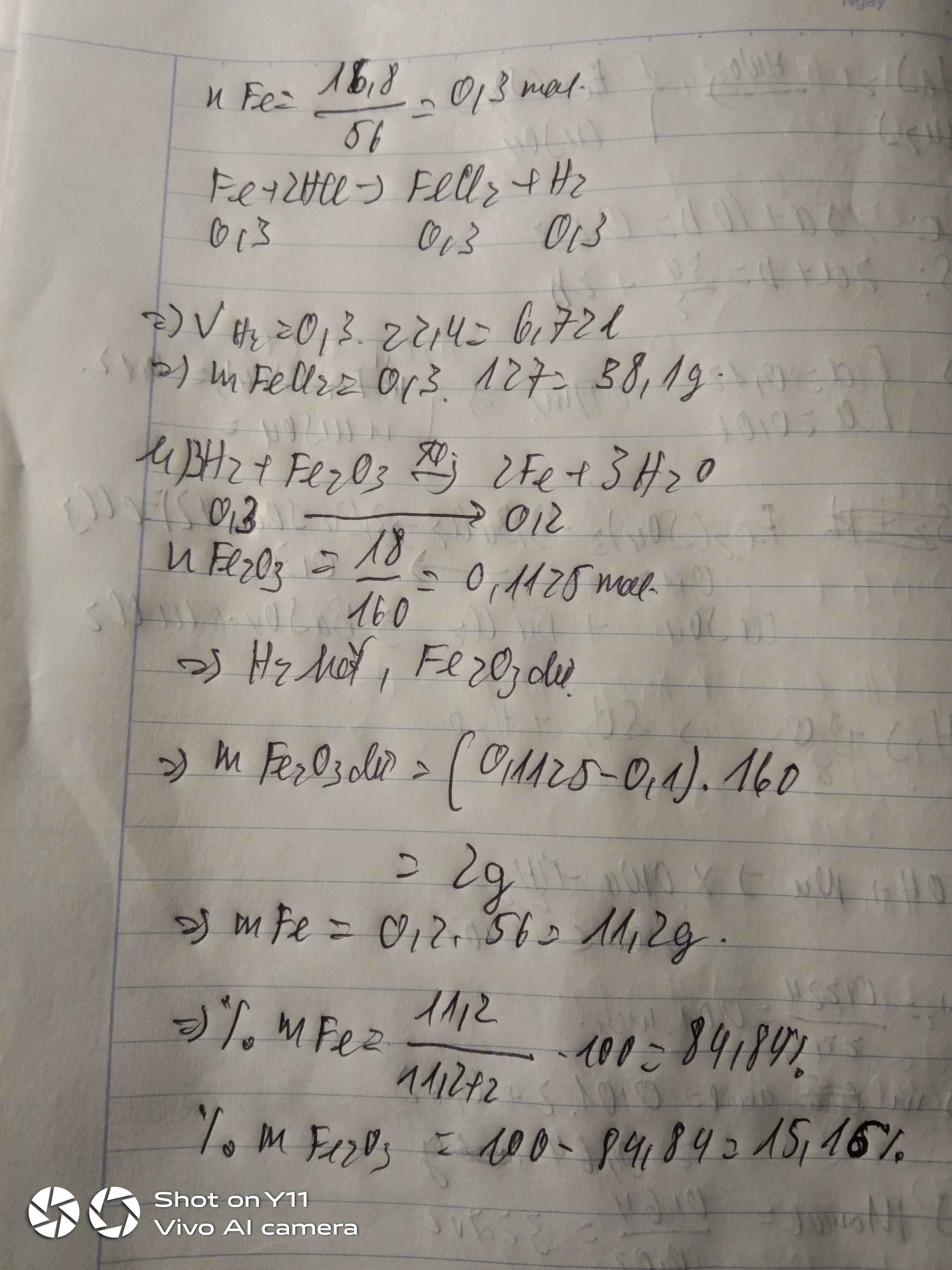

cảm ơn nha