Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3KCl + 6KOH → 5KCl + KCl O 3 + 4 H 2 O
Trong các phản ứng trên, clo vừa là chất oxi hoá, vừa là chất khử. Đó là các phản ứng tự oxi hoá, tự khử (hay còn gọi là phản ứng tự oxi hoá - khử).

Những cặp chất xảy ra phản ứng oxi hoá - khử :
(1)
(2) MnO2 + 4HCl > MnCl2 + Cl2 + 2H2O
b) Trong phản ứng (1) :
- Nguyên tử hiđro nhường electron là chất khử, sự nhường electron của H2 được gọi là sự oxi hoá nguyên tử hiđro.
- Ion đồng nhận electron, là chất oxi hoá. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
Trong phản ứng (2) :
- Ion Clo nhường electron là chất khử. Sự nhường electron của Cl được gọi là sự oxi hoá ion clo.
- Ion Mn nhận electron là chất oxi hoá. Sự nhận electron của ion Mn được gọi là sự khử ion Mn.

nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) = CM(MnCl2)CM(MnCl2) = CM(NaClO) =0,80,50,80,5 = 1,6 mol/l
CM(NaOH)dư = 2.1,60,52.1,60,5 = 0,8 mol/l

Phương trình hóa học của phản ứng:
Cl2 + 2NaI → 2NaCl + I2
71g (2 x 127)g
X g 12,7g
X = 3,55g
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
(4 x 36,5g) 71g
Y g 3,55 g
Y = 7,3g
Khối lượng HCl cần dùng là 7,3g

Gọi chung Cl2 và Br2 là X2, 2 bazo là ROH
X2 + 3ROH → 2RX + RXO3 + 3H2O
X2 + 2ROH→ RX + RXO + H2O
nROH = 0.5 mol
nX2 = 0.25 mol
→ Phản ứng xảy ra là phản ứng 2 (nROH = 2nX2)
Cl2 phản ứng trước Br2
X2 + 2ROH→ RX + RXO + H2O
→ Cl2 + 2ROH → NaCl + NaClO + H2O
----0.1-----0.2--------0.1
mH2O = 0.1 x 18 = 1.8g
nROH = 0,5 → mROH = 24.8g (0.2 NaOH, 0.3 KOH)
→ nROH = 0,2 → mROH = 9.92g
[m] mRCl = mCl2 + mROH p/ứ - mH2O
= 7.1 + 9.92 - 1.8 = 15,22.
1.
nCl2 = \(\frac{0,896}{22,4}\) = 0,04 (mol) , nNaOH = 1.0,2 = 0,2 (mol)
............Cl2 + 2NaOH → NaCl + NaClO + H2
Đầu.. 0,04........0,2
Pư .......0,04.......0,08............0,04.........0,04.........0,04
Spư......0............0,16............0,04.........0,04.........0,04
CM NaCl = \(\frac{0,04}{0,2}=0,2M\)
CM NaClO = CM NaCl = 0,2 M
CM NaOH = \(\frac{0,12}{0,2}=0,6M\)

Các chất có thể đóng vai trò chất oxi hoá là S, SO 2 , H 2 SO 3 . Thí dụ
a) S + 2Na → Na 2 S
b) SO 2 + 2 H 2 S → 3S + 2 H 2 O
c) H 2 SO 3 + 2 H 2 S → t ° 3S + 3 H 2 O
Các chất có thể đóng vai trò chất khử là S, H 2 S , SO 2 , H 2 SO 3 . Thí dụ
a) S + O 2 → t ° SO 2
b) H 2 S + Cl 2 → S + 2HCl
c) SO 2 + Br 2 + 2 H 2 O → H 2 SO 4 + 2HBr
d) 5 H 2 SO 3 + 2 KMnO 4 → 2 H 2 SO 4 + K 2 SO 4 + 2Mn SO 4 + 3 H 2 O

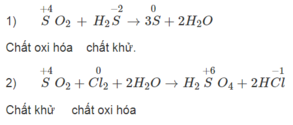
ở (1) SO 2 đóng vai trò là chất khử
ở (2) SO 2 đóng vai trò là chất oxi hóa.
3 Cl 2 + 2KOH → KCl + KClO + 3 H 2 O
Trong các phản ứng trên, clo vừa là chất oxi hoá, vừa là chất khử. Đó là các phản ứng tự oxi hoá, tự khử (hay còn gọi là phản ứng tự oxi hoá - khử).