Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn D
Ban đầu có nCO2 = 0,15 và tổng nOH– = 0,17 → 1 < nOH–/nCO2 < 2 → Tạo cả CO32– và HCO3–
→ nCO32– = nOH– – nCO2 = 0,17 – 0,15 =0,02 < 0,06 (nBa2+) → Tạo 0,02 BaCO3
Vậy m = 0,02 x 197 = 3,94.

Đáp án : B
nCO2 = 0,15 mol ; nOH = 0,17 mol
=> nCO3 = nOH - nCO2 = 0,02 mol < nBa = 0,06 mol
=> nBaCO3 = 0,02 mol => m = 3,94g

Đáp án B
nCaCO3 = 20: 100 = 0,2 mol. Vì Ca(OH)2 dư nên chỉ có phản ứng tạo muối trung hòa.
Ca(OH)2 + CO2 → CaCO3 + H2O
Mol 0,2 ← 0,2
=> VCO2 = 0,2.22,4 = 4,48 lit

Đáp án C
n C O 3 2 - = 0,2 mol; n H C O 3 - = 0,3 mol.
→ tỉ lệ 2 : 3.
→ 2x và 3x là số mol CO32– và HCO32– đã phản ứng
→ n H + = 2x.2 + 3x = 0,42 => x = 0,06 → n C O 2 = 2x + 3x = 0,3 mol.
Có n O H - = 0,36
Xét tỉ lệ T = n O H - n C O 2 thấy tạo ra đồng thời 2 muối CO32– và HCO3–.
→ n C O 3 2 - = 0,06; n H C O 3 - = 0,24
n B a 2 + = 0,08 → n B a C O 3 = 0,06 → m B a C O 3 = 11,82 gam.

Chọn C.
Khi cho từ từ X vào KHSO4 thì:
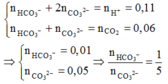
Khi Y tác dụng với Ba(OH)2 dư thì kết tủa thu được là
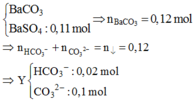
Vậy trong X có KHCO3 (0,03 mol) và Na2CO3 (0,15 mol) Þ m = 18,9 (g)
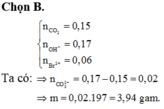
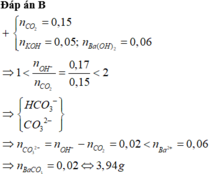

Chọn đáp án B