Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Ta có nC2H2 = 0,04 mol, nH2 = 0,06 mol
Bảo toàn khối lượng → mX = m bình tăng + mZ
→ mbình tăng = 0,04.26 + 0,06.2-4,5.2.0,04 = 0,8 gam

\(\left\{{}\begin{matrix}n_{C_2H_2}+n_{H_2}=\dfrac{2,24}{22,4}\\\dfrac{n_{C_2H_2}}{n_{H_2}}=\dfrac{2}{3}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{C_2H_2}=0,04\\n_{H_2}=0,06\end{matrix}\right.\)
\(m_Z=4,5\cdot2\cdot0,04=0,36g\)
BTKL: \(m_X=m_{bìnhtăng}+m_Z\)
\(\Rightarrow0,04\cdot26+0,06\cdot2=m_{bìnhtăng}+0,36\)
\(\Rightarrow m_{bìnhtăng}=0,8g\)
Chọn B

Đáp án D
Vì hỗn hợp X có nC2H2 = nC2H4
→ quy hh X về C2H3 và H2
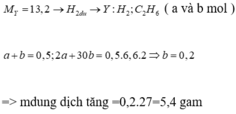

Chọn đáp án C
Ta có:mX=0,15.16+ 0,09.26+0,2.2=5,14gam
+ Theo ĐLBTKlg: mX = mY + mZ ⇒ mZ = mX – mY = 5,14 – 0,82 = 4,32 gam.
+ Mà: dZ/H2 = 8 ⇒ MY = 16/
⇒ nZ = mZ ÷ MZ = 4,32 ÷ 16 = 0,27 mol
⇒Thể tích của hh Z: V = 0,27 × 22,4 = 6,048 lít
⇒ Chọn C

Đáp án C
Một bình kín chứa 0,04 mol C2H2; 0,06 mol H2, một ít Ni.
Nung → hhY.
hhY + Br2 dư thì có 0,04 mol hhZ thoát ra. dZ/H2 = 4,5.
• Theo bảo toàn khối lượng: mC2H2 + mH2 = mbình brom tăng + mZ
→ mbình brom tăng = 0,04 x 26 + 0,06 x 2 - 0,04 x 9 = 0,8 gam

Đáp án D
Hướng dẫn
mY = 0,06.26 + 0,04.2 = 1,64 g; mZ = 0,02.16 = 0,32 g
m↑ = mY – mZ = 1,64 – 0,32 = 1,32 g

Đáp án D
nX = 1 mol; MX = 5,5.4 = 22
nZ = 0,2 mol; MZ = 11,5.2 = 23
BTKL: m bình Br2 tăng = mX – mZ = 1.22 – 0,2.23 = 17,4 gam
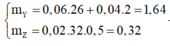
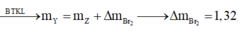
nX = 0,1 mol.
Các phản ứng xảy ra:
Từ tỉ lệ thể tích tính được
Khối lượng hỗn hợp đầu
Khối lượng khí thoát ra
Áp dụng định luật bảo toàn khối lượng ta có:
Khối lượng bình brom tăng thêm
m1 =m~ m2 = 1,16 - 0,36 = 0,8 gam
Đáp án B.