Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\)
\(BTe:\) \(2n_{Fe}+2n_{Zn}=2n_{H_2}\)
\(BTKL:\) \(56n_{Fe}+65n_{Zn}=18,6\)
\(\Rightarrow\left\{{}\begin{matrix}Fe:0,1mol\\Zn:0,2mol\end{matrix}\right.\)\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,1\cdot56=5,6g\\m_{Zn}=65\cdot0,2=13g\end{matrix}\right.\)

- Viết đúng ptpư:
\(Fe+4HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\)
\(3Cu+8HNO_3\rightarrow2Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(nNO=0,04\left(mol\right)\)
Gọi nFe là x(mol) ; nCu là y(mol)
ta có hệ pt:
\(\left\{{}\begin{matrix}m_{hh}=56x+64y=3,04\\nNO=x+\dfrac{2}{3y}=0,04\end{matrix}\right.\)
Giải hệ ta được: x = 0,02 mol ; y = 0,03 mol
\(\Rightarrow mFe=0,02.56=1,12\left(g\right)\)
\(mCu=0,03.64=1,92\left(g\right)\)

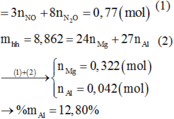


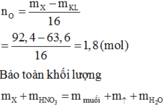

nH2=0,1 mol
Fe + 2HCl → FeCl2 + H2
0,1 mol 0,1 mol
mFe=0,1.56=5,6g
%mFe=\(\frac{5,6}{26}\).100=21,5%
m(feo và fe3o4)=26-5,6=20,4g
ta có phương trình cho nhận electron
Fe+2 ---------> Fe+3 + 1e N+5 + 3e-----------> N+2
x mol x mol 0,45 mol 0,15 mol
Fe3+8/3 ------------> 3Fe+3 + 1e
y mol y mol
Fe0 ------------> Fe+3 + 3e
0,1 mol 0,3mol
ta có hệ phương trình
\(\begin{cases}72x+232y+5,6=26\\0,3+x+y=0,45\end{cases}\) =>\(\begin{cases}x=0,09\\y=0,06\end{cases}\)
mFeO=0,09.72=6,48 g %mFeO=\(\frac{6,48}{26}.100=24,9\%\)
mFe3O4=13,92g %mFe3O4= 100%-(21,5%+ 24,9%)=53,6%