Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 2. \(n_{Cl_2}=\frac{11,2}{22,4}=0,5\left(mol\right)\);\(n_{NaI}=\frac{60}{150}=0,4\left(mol\right)\)
PTHH: \(Cl_2+2NaI\rightarrow2NaCl+I_2\uparrow\)
TheoPT:1..........2.........(mol)
Theo ĐB:0,5......0,4
Lập tỉ lệ: \(\frac{0,5}{1}>\frac{0,4}{2}\)=> Cl2 dư, NaI phản ứng hết
Theo phương trình : \(n_{I_2}=\frac{1}{2}n_{NaI}=0,2\left(mol\right)\)
\(n_{Cl_2\left(pứ\right)}=\frac{1}{2}n_{NaI}=0,2\left(mol\right)\)
\(n_{Cl_2\left(dư\right)}=0,5-0,2=0,3\left(mol\right)\)
Cl2 dư phản ứng với I2 vừa sinh ra
PTHH: \(5Cl_2+I_2+6H_2O\rightarrow10HCl+3HIO_3\)
Lập tỉ lệ giữa Cl2 và I2: \(\frac{0,3}{5}< \frac{0,2}{1}\)=> I2 dư
Theo PT : \(n_{I_2\left(pứ\right)}=0,06\left(mol\right)\)
\(\Rightarrow n_{I_2\left(dư\right)}=0,2-0,06=0,14\left(mol\right)\)
Vậy khối lượng I2 sau phản ứng: \(m_{I_2\left(dư\right)}=0,14.127.2=35,56\left(g\right)\)

Đáp án B
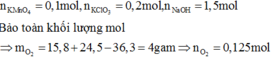
Khi cho hỗn hợp Y phản ứng với HCl đặc sẽ xảy ra phản ứng oxi hóa – khử tạo ra Cl2
![]()
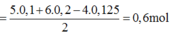


Em có thể tham khảo cách giải sau:
Ta có: mO2 = (15,8 + 24,5)-36,3 = 4 gam. => nO2 = 0,125 mol.
nKMnO4 = 0,1 mol, nKClO3 = 0,2 mol.
Mn7+ + 5e -> Mn2+
Cl5+ + 6e -> Cl-1
2O2- -> O2 + 4e
2Cl-1 -> Cl2 + 2e
Bảo toàn electron, ta có: 0,1*5 + 0,2*6 = 0,125*4 + 2*nCl2
=> nCl2 =0,6 mol.
3Cl2 + 6NaOH -> 5NaCl + NaClO3 + 3H2O (vì đun nóng).
Bđ 0,6 1,5
P/ư 0,6 1,2 1,0 0,2
Sau p/ư 0 0,3 1,0 0,2.
=> m Rắn =0,3*40 + 1,0*58,5 + 0,2*106,5 = 91,8 gam.

Đặt : nKMnO4 = 3a(mol)
nKClO3 = 4a (mol)
mX = 3a * 158 + 4a * 122.5 = 48.2 (g)
=> a = 0.05
BTKL :
mO2 = 48.2 - 40.2 = 8 (g)
nO2 = 8/32 = 0.25 (mol)
BT e :
5nKMnO4 + 6nKClO3 = 4nO2 + 2nCl2
=> nCl2 = 5*0.15 + 6*0.2 - 4*0.25 = 0.95 (mol)
VCl2 = 21.28 (l)
Chúc em học tốt và có những trải nghiệm mới tại hoc24.vn !

Gọi \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\\n_{Al}=c\left(mol\right)\end{matrix}\right.\) => 65a + 56b + 27c = 10,65 (1)
PTHH: Zn + 2HCl --> ZnCl2 + H2
Fe + 2HCl --> FeCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
=> \(n_{H_2}=a+b+1,5c=\dfrac{5,04}{22,4}=0,225\left(mol\right)\) (2)
PTHH: Zn + Cl2 --to--> ZnCl2
2Fe + 3Cl2 --to--> 2FeCl3
2Al + 3Cl2 --to--> 2AlCl3
=> \(n_{Cl_2}=a+1,5b+1,5c=\dfrac{5,6}{22,4}=0,25\left(mol\right)\) (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,05\left(mol\right)\\c=0,05\left(mol\right)\end{matrix}\right.\) => \(\left\{{}\begin{matrix}m_{Zn}=0,1.65=6,5\left(g\right)\\m_{Fe}=0,05.56=2,8\left(g\right)\\m_{Al}=0,05.27=1,35\left(g\right)\end{matrix}\right.\)
a) \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{6,5}{10,65}.100\%=61,033\%\\\%m_{Fe}=\dfrac{2,8}{10,65}.100\%=26,291\%\\\%m_{Al}=\dfrac{1,35}{10,65}.100\%=12,676\%\end{matrix}\right.\)
b) nHCl = 2a + 2b + 3c = 0,45 (mol)
=> mHCl = 0,45.36,5 = 16,425 (g)
=> \(a\%=C\%=\dfrac{16,425}{200}.100\%=8,2125\%\)
c) mdd sau pư = 10,65 + 200 - 0,225.2 = 210,2 (g)
=> \(\left\{{}\begin{matrix}C\%_{ZnCl_2}=\dfrac{0,1.136}{210,2}.100\%=6,47\%\\C\%_{FeCl_2}=\dfrac{0,05.127}{210,2}.100\%=3,02\%\\C\%_{AlCl_3}=\dfrac{0,05.133,5}{210,2}.100\%=3,176\%\end{matrix}\right.\)

Gọi số mol Mg, Fe, Al là a, b, c
=> 24a + 56b + 27c = 23,8
PTHH: Mg + 2HCl --> MgCl2 + H2
a------------------------->a
Fe + 2HCl --> FeCl2 + H2
b------------------------->b
2Al + 6HCl --> 2AlCl3 + 3H2
c------------------------->1,5c
=> a + b + 1,5c = \(\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
PTHH: Mg + Cl2 --to--> MgCl2
a-->a
2Fe + 3Cl2 --to--> 2FeCl3
b--->1,5b
2Al + 3Cl2 --to--> 2AlCl3
c--->1,5c
=> \(a+1,5b+1,5c=\dfrac{20,16}{22,4}=0,9\left(mol\right)\)
=> a = 0,3; b = 0,2; c = 0,2
=> \(\left\{{}\begin{matrix}m_{Mg}=0,3.24=7,2\left(g\right)\\m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)





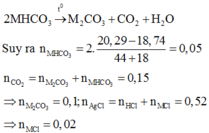
2Fe +3Cl2 -->2FeCl3
nCl2= 5,6 \22,4 =0,25 mol
=>CL2 dư
nFeCl3=6,5\162,5=0,04 mol
theopt nFe =0,04 mol
mfe =0,04 .56 =2,24 g=m
Thiếu trường hợp!