Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
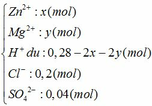
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
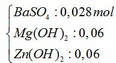
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
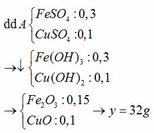

Gọi số mol của BaO, BaCO3, NaHCO3 trong 30,19g hh lần lượt là x, y, z
Có 153x + 197y + 84z = 30,19
Phần 1:
BaO + H2O → Ba(OH)2
x x
OH- + HCO3- → CO32- + H2O
Ba2+ + CO32- → BaCO3
n kết tủa = 0,11
Phần 2:
BaCO3 →BaO + CO2
y y
2NaHCO3 → Na2CO3 + H2O + CO2
z z/2 z/2
=> mCO2 + mH2O = 30,19 – 26,13 = 4,06
=> 44 (y + z/2) + 18 . z/2= 4,06
TH1: Ba tạo kết tủa hoàn toàn thành BaCO3 và NaHCO3 dư
=> nBaCO3 = nBaCO3 + nBaO = 0,11 => Không thỏa mãn
TH2: Ba(OH)2 dư và NaHCO3 hết
=> x + y = 0,11 và y + z = 0,11
=> x = 0,1; y = 0,05 và z = 0,06
a.
hh Y gồm BaO: 0,15 mol; Na2CO3: 0,03 mol
BaO + H2O → Ba(OH)2
0,15 0,15
Ba(OH)2 + Na2CO3 → BaCO3 + 2NaOH
0,15 0,03 0,03 0,06
=> m kết tủa = 0,03 . 197 = 5,91g
m dd = m chất rắn + mH2O – mBaCO3 = 26,13 + 79,78 – 5,91 = 100
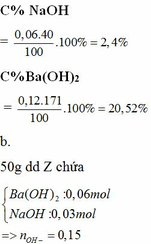
nAl2(SO4)3 = 0,02 => nAl3+ = 0,04; nSO42- = 0,06
Ba2+ + SO42- → BaSO4
0,06 0,06 0,06
nAl(OH)3 = 0,01 => mAl(OH)3 = 0,78g
m = 0,78 + 0,06 . 233 = 14,76g

a) Nhận xét: 33,84g X > 16g rắn → kim loại còn dư.
Chú ý: sau một thời gian ám chỉ các chất tham gia đều dư.
Giả sử số mol của Mg, Fe lần lượt là x, y
Tăng giảm khối lượng: (64 – 24) . x + (64 – 56) . y = 38,24 – 33,84 (1)
Chất rắn bao gồm MgO: x; Fe2O3: 0,5y; CuO: a – x – y
=> 40x + 160 . 0,5y + 80(a – x – y) = 16 (2)
Từ (1) và (2) => 10a + y = 2,55
amax <=> y = 0 => amax = 0,255
b) giá trị a đạt max thì Fe chưa tham gia pứ.
Giả sử số mol Mg dư là: z (mol) 19,12g Z cho 0,48 mol SO2 → 38,24g Z cho 0,96 mol SO2
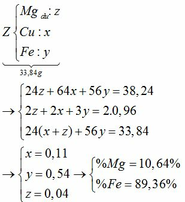





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

Phương trình:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
FeSO4 + 2NaOH → Na2SO4 + Fe(OH)2↓
Fe2(SO4)3 + 6NaOH → 3Na2SO4 + 2Fe(OH)3↓
2Fe(OH)2 + ½ O2 → Fe2O3 + 2H2O
2Fe(OH)3 → Fe2O3 + 3H2O
Fe2O3 + 3CO → 2Fe + 3CO2↑
CO2 + Ca(OH)2 → CaCO3↓ + H2O
3CO2 + Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2 → CaCO3 + CO2↑ + H2O






Trường hợp 2: phản ứng tạo ra 2 loại muối
SO2 + MOH \(\rightarrow\) MHSO3
x mol x mol
SO2 + 2MOH \(\rightarrow\) M2SO3 + H2O
y mol 2y mol y mol
nSO2 < nNaOH < 2nSO2 => 0,2 < a < 0,4
Ta có hệ phương trình: x+ y= nSO2 và x+ 2y =nMOH
=> y= nMOH - nSO2 = 0,4 - a= nH2O sinh ra
Theo định luật bảo toàn khối lượng:
mSO2 + mNaOH + mKOH = m chất tan + mH2O sinh ra
64.a+0,3.40+0,1.56 = 30,08 + 18.(0,4-a)
=> a= 0,24 ( thỏa mãn) => V= 5,376 lít
Xét phản ứng giữa hỗn hợp A với H2SO4 đặc
R2SO3 + H2SO4 \(\rightarrow\)R2SO4 + SO2 + H2O
2RHSO3 + H2SO4 \(\rightarrow\)R2SO4 + 2SO2+ H2O
Từ 2 phương trình trên ta thấy: nhỗn hợp A = nSO2= 0,24
Tính được M ( trung bình) của hỗn hợp A bằng 115
=> R + 81 < 115 < 2R + 80
=> 17,5 < R < 43
=> R là Na (M = 23)
Xét phản ứng giữa Na với dd HCl:
nNa= 0,5 mol; nHCl = 0,4 mol
Nadư + HClhết \(\rightarrow\) NaCl + H2O
0,4 mol 0,4 mol 0,4 mol
nNadư = 0,5-0,4 = 0,1 mol
2Na + 2H2O \(\rightarrow\) 2NaOH + H2
0,1 mol 0,1 mol
Dung dịch Y chứa: 0,4 mol NaCl và 0,1 mol NaOH
NaCl + AgNO3 \(\rightarrow\) AgCl + NaNO3
0,4 mol 0,4 mol
NaOH + AgNO3\(\rightarrow\)AgOH+ NaNO3
0,1 0,1
2AgOH\(\rightarrow\)Ag2O + H2O
0,1 0,05
Kết tủa thu được gồm 0,4 mol AgCl và 0,05 mol Ag2O có tổng khối lượng là 69 gam
- PTHH: 2Al + 3H2SO4 \(\rightarrow\) Al2 (SO4)3 + 3H2 (1)
MgO + H2SO4 \(\rightarrow\) MgSO4 + 2HO (2)
2NaOH+ H2SO4 \(\rightarrow\) Na2SO4 + 2H2O (3)
2NaOH+ MgSO4 \(\rightarrow\) Mg(OH)2 + Na2SO4 (4)
6NaOH+ Al2(SO4)3\(\rightarrow\) 3Na2SO4 + 2Al(OH)3 (5)
NaOH + Al(OH)3 \(\rightarrow\) NaAlO2 + 2H2O (6)
Mg(OH)2 \(\rightarrow\) MgO + H2O (7)
CO2 + NaOH \(\rightarrow\) NaHCO3 (8)
CO2 + NaAlO2 + 2H2O \(\rightarrow\) Al(OH)3 + NaHCO3 (9)
nH2SO4= \(\dfrac{163,68.28,74}{100.98}\)= 0,48 mol
Ta có: nH2 = \(\dfrac{6,048}{22,4}\)= 0,27 mol
Theo (1): nAl= \(\dfrac{2}{3}\)0,27 = 0,18 mol
- Ta coi dung dịch Y có 2 phần: + Phần 1 là dd Y ban đầu
+ Phần 2 là dd Y có khối lượng 100g
Kết tủa T là Al(OH)3 có số mol = 9,36/37 = 0,12 mol
Gọi k là tỉ số giữa phần 1 và phần 2
Suy ra k= 0,18/0,12= 1,5
\(\Rightarrow\) \(\dfrac{m+163,68-0,54}{120}\)= 1,5
\(\Rightarrow\) m= 16,86 (gam)
- Ở phần 1: mol axit dư= (16,86 + 163,68 - 0,54). 4,9/(100.98)= 0,09 mol
\(\rightarrow\) mol axit pư với MgO= mol MgO = 0,48-0,27-0,09 = 0,12 mol
Vậy phần trăm về khối lượng từng chất trong hỗn hợp ban đầu là:
%mAl = \(\dfrac{0,18.27}{16,86}\)100% = 28,82%
%mMgO= \(\dfrac{0,12.40}{16,86}\)100%= 28,47%
%mMgSO4 = 100% - 28,82% - 28,47% = 42,71%
Tìm x: Tổng mol MgSO4 trong dd Y ban đầu là
nMgSO4 = nMgO + nMgSO4 (bd)
= 0,12 + (16,9860 - 4,86- 4,8) : 120 = 0,18 mol
Do: nMgSO4 (p1) = 1,5n MgSO4 (p2)
Ở phần 1 của dung dịch Y:
\(\Rightarrow\)MgSO4 (p2) = \(\dfrac{0,18}{1,5}\)= 0,12 mol
Theo PT (4,7)
a=mMgO = 0,12.40 = 4,8 gam
nNaOH= 0,3 mol; nKOH= 0,1 mol
Xết pư giữa a mol SO2 với dd chứa 0,3 mol NaOH và 0,1 mol KOH ( quy về MOH: 0,4 mol)
+ Trường hợp 1: MOH dư
SO2 + 2MOH \(\rightarrow\)M2SO3 + H2O
a 2a a
nH2O sinh ra= a mol và 2a < 0,4 => a <0,2
Theo ĐLBTKL:
mSO2 + mNaOH + mKOH = m chất tan + mH2O sinh ra
64.a+ 0,3.40 + 0,1.56 = 30,08 + a.18
=> a= 0,27 ( vô lý)