Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Do kim loại Cu dư nên dung dịch Y không thể có Fe3+
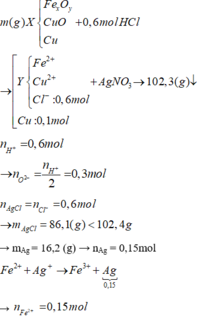
Áp dụng định luật bảo toàn điện tích trong dung dịch Y → nCu2+ = 0,15 mol
→ m = mFe + mO + mCu = 0,15. 56 + 0,3 . 16 + 0,15 . 64 + 6,4 = 29,2 (g)

Đáp án C
Do kim loại còn dư nên không có muối
![]()
Bảo toàn nguyên tố Clo: ![]()
![]()
![]()
![]()
![]()
![]()
Bảo toàn nguyên tố Fe và Cu
![]()
![]()

Đáp án C
Do kim loại còn dư nên không có muối ![]()
Bảo toàn nguyên tố Clo: ![]()
![]()
=> kết tủa chứa Ag ![]()
![]()
![]()
Bảo toàn nguyên tố Hidro và Oxi:
![]()
Bảo toàn nguyên tố Fe và Cu
m = 0,25.56 + 0,2.64 + 0,45.16 + 96 = 43,6 (g)

Đáp án A.
X + HCl dư → FeCl2 + CuCl2 + HCl (dư) + H2O + Cu (dư),
||⇒ quy đổi quá trình → X gồm FeO (tạo FeCl2) + CuO (tạo CuCl2) + Cu (dư).
a mol FeO + b mol CuO + 0,27m Cu; trong đó ∑nO trong oxit = 0,01m (mol).
⇒ giải: a + b = 0,01m và 72a + 80b = m – 0,27m ||⇒ a = 0,00875m và b = 0,0125m.
Giải còn lại, ta gọi nFeCl2 = 7x mol → nCuCl2 = x mol → nHCl dư = 1 – 16x) mol.
Gộp quá trình:
(FeCl2, CuCl2, HCl) + AgNO3 → AgCl 1,0 mol) + (Fe(NO3)3; Cu(NO3)2) + NO + H2O.
165,1 gam tủa gồm Ag và AgCl nhưng về mặt nguyên tố gồm 1 mol Cl → còn lại là 1,2 mol Ag.
nNO = nHCl ÷ 4 = 0,25 – 4x) mol; lại có nFe(NO3)3 = 7x mol; nCu(NO3)2 = x mol
⇒ bảo toàn nguyên tố N có: 21x + 2x + 0,25 – 4x) = 1,2 ⇒ x = 0,25 mol.
Theo đó: m = 800b = 800x = 40 gam.


Khi cho X tác dụng với HCl và dung dịch Y tác dụng với AgNO3 thì ta có hệ sau:
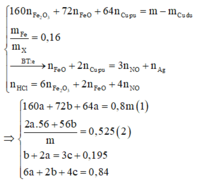
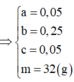
Đáp án B
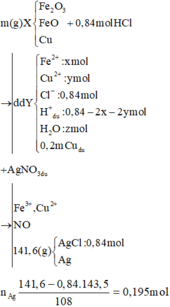


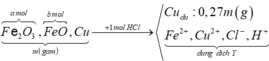
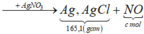
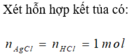
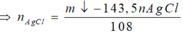
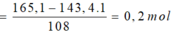

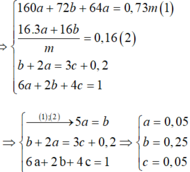
Do Cu dư sau pư⟶hỗn hợp Y chứa muối Fe2+
nCu trong X = 0,1; nAgCl = 0,6
BTKL ⟶ m = 29,2
Đáp án C