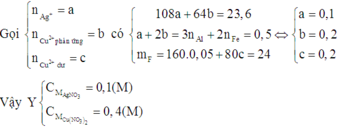Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
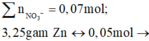 cuối cùng Y cho 0,035 mol
Z
n
(
N
O
3
)
2
cuối cùng Y cho 0,035 mol
Z
n
(
N
O
3
)
2
Bảo toàn khối lượng lần 1: mchất tan trong X
![]()
Bảo toàn khối lượng lần 2||

Đáp án D
Có Fe : m g Zn : 0 , 05 mol + A g N O 3 : 0 , 03 m o l C u N O 3 2 : 0 , 02 m o l → 7 , 735 Ag : 0 , 03 mol Cu : 0 , 02 mol Fe : x mol Zn : y mol
⇒ 56 x + 65 y = 7 , 735 - 108 . 0 , 03 - 64 . 0 , 02 = 3 , 215 → B T e 2 . ( 0 , 05 - y ) = 1 . 0 , 03 + 2 . 0 , 02 ⇒ y = 0 , 015 x = 0 , 04 ⇒ m = 56 . 0 , 04 = 2 , 24 g

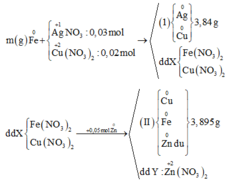
Từ sơ đồ phản ứng ta thấy Fe từ số oxi hóa 0 vẫn về 0
=> ne( Ag+, Cu2+ nhận) = ne ( Zn nhường)
Mà ∑ ne ( Ag+, Cu2+ nhận) = 0,03.1 + 0,02.2 = 0,07 < ne ( Zn nhường) = 0,1 (mol)
=> Zn còn dư sau phản ứng
=> nZn pư = ½ ne nhận = ½. 0,07 = 0,035 (mol)
=> nZn dư = 0,05 – 0,035 = 0,015 (mol)
mFe + mAg bđ + mCu bđ + mZn dư = mAg+Cu (I) + mCu + Fe + Zn (II)
=> mFe = mAg+Cu (I) + mCu + Fe + Zn (II) - ( mAg bđ + mCu bđ + mZn dư )
=> mFe = 3.84 + 3,895 – (0,03.108 + 0,02.64 + 0,015. 65)
mFe = 2,24 (g)
Đáp án B

Đáp án A
![]()
↔ 0,05 mol => cuối cùng Y cho 0,035 mol Z n ( N O 3 ) 2
Bảo toàn khối lượng lần 1: ![]() = 7,26 gam
= 7,26 gam
Bảo toàn khối lượng lần 2: => m = 7,26 + 3,84 - 0,03.170 - 0,02.188 = 2,240 gam

Đáp án A
![]()
→ cuối cùng Y cho 0,035 mol Z n ( N O 3 ) 2
Bảo toàn khối lượng lần 1:
![]() = 7,26 gam
= 7,26 gam
Bảo toàn khối lượng lần 2:
![]()
= 2,240 gam

Đáp án A
nZn = 0,06 mol > ½ nNO3
=> Zn dư , dung dịch muối Y chỉ có Zn(NO3)2 với số mol là 0,04 mol
Bảo toàn khối lượng :
mZn + mY = mZn(NO3)2 + mrắn => my = 9,8g
Và : mCu + mAgNO3 = mX + mY
=> mCu = m = 3,2g

Đáp án D
Vì dung dịch C đã mất màu hoàn toàn nên cả Ag+ và Cu2+ đều phản ứng hết.
Mà B không tan trong HCl nên B chỉ chứa Ag và Cu. Do đó cả Al và Fe đều phản ứng hết.
Suy ra cho X vào A thì cả 4 chất đều phản ứng vừa đủ.
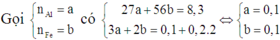
Vì dung dịch E đã nhạt màu nên Ag+ đã phản ứng hết và Cu2+ đã phản ứng một phần.
Do đó D chứa Ag và Cu.
Dung dịch E chứa Al3+, Fe2+ và Cu2+ dư. Khi đó E chứa Fe(OH)2 và Cu(OH)2
Suy ra F chứa Fe2O3 và CuO