Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
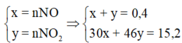
![]()
Bảo toàn ne =>2nCu = 3nNO + nNO2 =>nCu = 0,4 => m = 25,6 => Chọn A.

Đáp án A
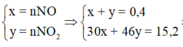
![]()
Bảo toàn ne =>2nCu = 3nNO + nNO2=> nCu = 0,4 => m = 25,6 => Chọn A.

Quy hỗn hợp thành hỗn hợp gồm Fe (a mol)và S (b mol)
=> 56a + 32b = 3,76
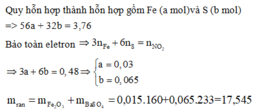
Đáp án D

145.625g kt= SO42- =0.625 = H2SO4 bđ ( do H+ NO3- chỉ khử S trong hh , SO42- của axit còn nguyên)
Dự đoán X chứa NH4+ nên hh khí cuối cùng có NO2,O2 của Nitrat kim loại ,N2O của NH4NO3. Còn lượng H2O bị Oxit KL hấp thụ hoàn toàn
2NO3 -> O2- + 2NO2 +1/2O2
a a a/4 (mol)
NH4NO3 -> H2O + N2O
b b (mol)
Giải hpt => a=1.24
b= 0.02
Đồng thời do a là mol gốc Nitrat của KL nên a cũng là tổng mol điện tích dương của KL
BTĐT ddY => NO3-= 1.26
=> ddX Cu2+
Mg2+
NH4+ 0.02
SO42- 0.625
NO3- 0.01
Đặt x,y,z lll mol NO2,NO,SO2
x+y+z=1.16
46x+30y+64z=49.6
*Quy hh đầu về Cu,Mg,S
Tác nhân H+ NO3- khiến:
Cu -> Cu2+
Mg-> Mg2+
S -> S+4 (SO2)
-> Bte: 1.24+ 4z= x+3y+0.02*8
Giải hpt => x=0.5
y=0.46
z= 0.2
=> HNO3= 0.99 (btN)
=> H2O=1.08 (btH)
BTKL => m= 38.88 => C
Cho Cô hỏi khối lượng 67,84 gam đó là khối lượng của khí hay là của chất rắn có khối lượng ko đổi?

Đáp án C
· X gồm 0,2539m (g) O và 0,7461m (g) kim loại.
· Hỗn hợp khí Z gồm CO dư và CO2
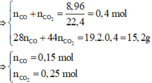
Þ Y gồm 0,7461m (g) kim loại và 0,2539m – 16.0,25 = 0,2539m – 4 (g) O
· Y + HNO3 → 0,32 mol NO + 3,456m g muối
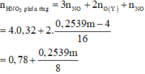
Þ Dung dịch T chứa
n NO 3 - = 0 , 78 + 0 , 2359 m 8 - 0 , 32 = 0 , 46 + 0 , 2359 m 8 ⇒ m muối = 0 , 7461 m + 62 . 0 , 46 + 0 , 2359 m 8 = 3 , 456 m ⇒ m = 38 , 43 g
Gần nhất với giá trị 38

Đáp án A

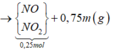
Chất rắn
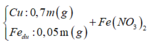
![]()
![]()

![]()
=> 0,225.56 = 0,3m - 0,05m => m = 50,4 (g)
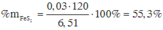



Đáp án A