Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

Số mol H3PO4: 0,050 x 0,50 = 0,025 (mol).
H3PO4 + 3NaOH → Na3PO4 + 3H2O
1 mol 3 mol
0,025 mol 3 x 0,025 mol
Thể tích dung dịch NaOH: 0,075 lít hay 75 ml

bạn có ghi bài trên lớp phần cấu tạo chất đủ không. co mình mượn chép lại mấy bài phần đó với

a) Ta có: Mật độ xác suất tìm thấy electron trong vùng không gian xung quanh hạt nhân nguyên tử:
D(r) = R2(r) . r2
= 416/729 . a0-5 . r2 . (2 - r/3a0)2 . e-2r/3a0 . r2
= 416/729 . a0-5 . (4r4 - 4r5/3a0 + r6/9a02) . e-2r/3a0
Khảo sát hàm số D(r) thuộc r
Xét: d D(r)/ dr = 416/729 . a0-5 . [(16r3 - 20r4/3a0 + 2r5/3a02) . e-2r/3a0 - (4r4 - 4r5/3a0 + r6/9a02) . 2/3a0 . e-2r/3a0 ]
= 416/729 . a0-5 . e-2r/3a0 . r3 . (16a03 - 28r/3a0 + 14r2/9a02 - 2r3/27a03)
= 832/19683 . a0-8 . e-2r/3a0 . r3 . (-r3 +21r2.a0 - 126r.a02 +216a03)
= - 832/19683 . a0-8 . e-2r/3a0 . r3 . (r - 6a0).(r - 3a0).(r - 12a0)
d D(r)/ dr = 0. Suy ra r =0; r =3a0 ; r = 6a0; r = 12a0
Với r = 0 : D(r) =0
r =3a0 : D(r) = 416/9 .a-1 . e-2
r =6a0 : D(r) = 0
r =12a0 : D(r) = 425984/9.a-1 . e-8
b) Ai vẽ câu này rồi cho up lên với, cám ơn mọi người trước nhé!
a)Mật độ xác suất có mặt electron tỷ lệ với |R3P|2.r2
D(r)=|R3P|2.r2 =D (r)=\(\frac{416}{729}\) .a0-5.(2r2- \(\frac{r^3}{3a_0}\)).\(^{e^{-\frac{2r}{3a_0}}}\)
Lấy đạo hàm của D theo r để khảo sát mật độ xác suất :
D' (r)= \(\frac{416}{729}\) .a0-5.2.(2r2-\(\frac{r^3}{3a_0}\)).(4r-\(\frac{r^2}{a_0}\)).\(^{e^{-\frac{2r}{3a_0}}}\)+\(\frac{416}{729}\) .a0-5.(2r2-\(\frac{r^3}{3a_0}\))2.(-\(\frac{2}{3a_0}\)).\(^{e^{-\frac{2r}{3a_0}}}\)
=\(\frac{832}{729}\). a0-6.\(^{e^{-\frac{2r}{3a_0}}}\). (2r2-\(\frac{r^3}{3a_0}\)) .[(4r-\(\frac{r^2}{a_0}\)).a0 -\(\frac{1}{3}\). (2r2-\(\frac{r^3}{3a_0}\))]
=\(\frac{832}{729}\). a0-6.\(^{e^{-\frac{2r}{3a_0}}}\).r3.(2- \(\frac{r}{3a_0}\)).(\(\frac{r^2}{9a_0}-\frac{5r}{3}+4a_0\))
=>D’(r)=0 => r=0 ,r=3a0 ,r=6a0 ,r=12a0.
Với:r=0 =>D(r)=0
r=3a0 =>D(r)=0
r=6a0 =>D(r)=\(\frac{416}{9a_0.e^2}\)
r=12a0=>D(r)=\(\frac{425984}{a_0.e^8}\)
b)

TH1: Cả 2 muối \(NaX\) và \(NaY\) đều pứ vs \(\text{AgNO3}\)
\(NaZ\) + \(AgNO_3\) \(\rightarrow\) \(NaNO_3\) + \(AgZ\)
TH2: 2 muối của X và Y lần lượt là \(NaF\) và \(NaCl\)
Mol \(AgCl\) =8,61/143,5 = 0,06mol
0,06<= 0,06
m\(NaCl\) = 0,06.58,5=3,51g
%m\(NaF\) = 2,52/6,03 .100% = 41,79%
Do AgF tan, khác các muối còn lại nên chia thành 2 trường hợp:
TH1: Hai muối ban đầu là NaF và NaCl —> nNaCl = nAgCl = 0,06 —> %NaF = 41,79%
TH2: Cả 2 muối đều tạo kết tủa:
m tăng = n muối (108 – 23) = 8,61 – 6,03 —> n muối = 0,03 —> M = 198,6 —> Halogen = M – 23 = 175,6: Vô nghiệm



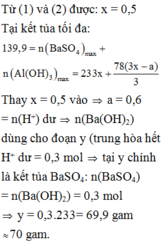
Chọn B.
Dung dịch Y có n A l 2 ( S O 4 ) 3 = V/3 = x m o l và n A l C l 3 = V 3 = x m o l .
⇒ n A l 3 + = 3 x m o l = n S O 4 2 -
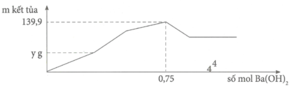
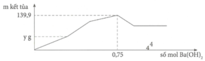
Tại n B a ( O H ) 2 = 0,75 mol => n O H - = 1,5 mol: lúc này cả 2 kết tủa tối đa với
n A l ( O H ) 3 = 1 / 3 n O H - = 0 , 5 m o l ⇒ n B a S O 4 m a x . 233 + 0 , 5 . 78 = 139 , 9 ⇒ n B a S O 4 m a x = 0 , 433 < 0 , 5 ⇒ v ô l ý
Chứng tỏ trong dung dịch Y còn H+ dư đoạn đồ thị đi lên đầu tiên đến y chỉ có 2 phản ứng là: H + + O H - → H 2 O ⇒ n O H - kết tủa hết Al3+ = 1,5 - a
⇒ n A l ( O H ) 3 m a x = 1 , 5 - a 3 ( 1 ) S O 4 2 - + B a 2 + → B a S O 4 (1)
Dung dịch Y ( : x mol, Cl-: x mol, H+: a mol)
Bảo toàn điện tích: n A l 3 + = 3 x - a 3 ⇒ n A l ( O H ) 3 m a x = 3 x - a 3 (2)
Từ (1) và (2), ta được: x = 0,5 mol
Tại kết tủa tối đa: 139 , 9 = n B a S O 4 m a x + n A l ( O H ) 3 m a x = 233 x + 78 ( 3 x - a ) 3
Thay x = 0,5 vào a = 0,6 mol = n(H+) dư n(Ba(OH)2) dùng cho đoạn y (trung hòa hết H+ dư = 0,3 mol tại y chính là kết tủa
BaSO4: n(BaSO4) = n(Ba(OH)2) = 0,3 mol
=>y = 0,3.233= 69,9 gam ≈ 70 gam.