Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nước clo dần dần bị mất màu theo thời gian, không bảo quản được lâu là do quá trình phân huỷ HClO :
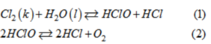
Phản ứng (2) làm cho nồng độ HClO giảm, cân bằng hoá học của phản ứng (1) chuyển dịch theo chiều thuận, clo sẽ phản ứng với nước cho đến hết, do đó nước clo không bền.

\(2NaBr + Cl_2 \to 2NaCl + Br_2\\ 2NaI + Cl_2 \to 2NaCl + I_2\\ n_{NaBr} + n_{NaI} = n_{NaCl} = \dfrac{2,94}{58,5} = 0,050256\)

Bạn tham khảo ở đây nha:Câu hỏi của Lê Quang Hiếu - Hóa học lớp 12 | Học trực tuyến
vì K+ và Na+ nên viết p.tử không chuẩn
a) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước vì nộng độ H+trong dd mới tạo thành nhỏ nên sẽ tác dụng từng nấc(vì chỉ từng giọt).lượng H+ chưa dư khi tác dụng với CO32- nên không thể tác dụng tiếp với HCO3- dẫn đến không có hiện tượng
H++CO32- -->HCO3-
b) khi cho H+ từ từ vào CO32- và HCO3- thì H+ td với CO32- trước. H+ tác dụng với CO32- còn dư tác dụng với 1 phần HCO3- tạo CO2 khí ko màu dd còn HCO3- tác dụng với OH- tạo CO32- td Ba2+ tạo kt trắng BaCO3
CO32-+H+-->HCO3-
HCO3-+H+-->H2O+CO2
HCO3-+OH-+Ba2+-->BaCO3+H2O(dư nên khi vậy ko dư ghi tỉ lệ Ba2+:OH-=1:2)
c)cho từ từ CO32- và HCO3- vào H+ thì pứ xảy ra đồng thời tạo đều tạo khí CO2 vì khi cho vào thì mt có nồng độ H+ lớn nên pứ xảy ra theo 2 nấc đồng thời
CO32-+2H+-->H2O+CO2
HCO3-+H+-->H2O+CO2

\(2NaBr + Cl_2 \to 2NaCl + Br_2\\ 2NaI + Cl_2 \to 2NaCl + I_2\\ n_{Cl_2} =\dfrac{1}{2}n_{NaCl} = \dfrac{1}{2}.\dfrac{23,4}{58,5} = 0,2(mol)\\ \Rightarrow V_{Cl_2} = 0,2.22,4 = 4,48(lít)\)

Chọn C
Phân tử khối của HCl nhỏ hơn của NaOH
=> phản ứng theo tỉ lệ mol 1 : 1 => HCl dư => Quỳ tím chuyển màu sang màu đỏ.

Kết tủa vàng chính là S
Trong môi trường axit, Mn+7 bị khử về Mn+2
Clo đẩy brom ra khỏi muối :
Cl 2 + 2NaBr → NaCl + Br 2
Brom tan vào nước tạo ra dung dịch màu vàng.
Tiếp tục cho clo đi vào thì nó oxi hoá brom :
5 Cl 2 + Br 2 + 6 H 2 O → 2HBr O 3 + 10HCl
Các axit tạo thành không màu, dung dịch của chúng là quỳ tím hoá đỏ.