Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Gọi 2 axit có công thức chung là RCOOH.
Khi tham gia phản ứng với Na → nancol + naxit = 2nH2 = 0,6 mol
Vì các chất trong hỗn hợp phản ứng este hóa vừa đủ với nhau → naxit = nancol = 0,3 mol
→ nRCOOCH3 = naxit = 0,3 mol → (R + 44 + 15). 0,3 = 25 →15 (CH3) < R = 24,333 < 29 (C2H5)
Vậy axit kế tiếp nhau là CH3COOH. Đáp án A.

Đáp án A
Gọi 2 axit có công thức chung là RCOOH.
Khi tham gia phản ứng với Na → nancol + naxit = 2nH2 = 0,6 mol
Vì các chất trong hỗn hợp phản ứng este hóa vừa đủ với nhau → naxit = nancol = 0,3 mol
→ nRCOOCH3= naxit = 0,3 mol → (R + 44 + 15). 0,3 = 25
→15 (CH3) < R = 24,333 < 29 (C2H5)
Vậy axit kế tiếp nhau là CH3COOH.

Đáp án C
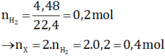
Khi thực hiện phản ứng este hóa axit và ancol phản ứng vừa đủ với nhau
→ naxit = nancol
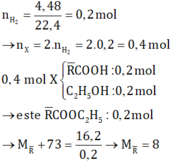
→ 2 axit là: HCOOH và CH3COOH

X : nH2 = 0,2
Vì 2 chất phản ứng vừa đủ tạo este nên naxit = nancol = neste = 0,2 mol
MRCOOC2H5 = 16,6/0,2 = 81 → R = 8
→ HCOOH, CH3COOH
→ Đáp án D

Gọi CTC ax: RCOOH
X: CH3OH và RCOOH
Gọi nCH3OH=a mol; nRCOOH=b mol
Đun nóng X các chất phản ứng vửa đủ với nhau => a=b
nH2=0,3 mol
=>Ta có a+b=0,6 mol
<=> a=b=0,3mol
Với H=100% => n este=0,3 mol=n ancol=n axit
M RCOOCH3=25/0,3
<=>R trung bình=73/3=24,33
Do R no,đồng đẳng kế tiếp => R1=15 và R2=29
=>2 axit là CH3COOH và C2H5COOH
cho mình hỏi là nH2=0.3 là của cả nH2(ancol) và nH2(axit) mà đúng không? vậy thì a=b=0.15 chứ nhỉ. nếu mình làm vậy thì nó lại không ra kq, vậy rốt cuộc tại sao có thể kết luận 0.3 đề cho không phải là tồng nH2?
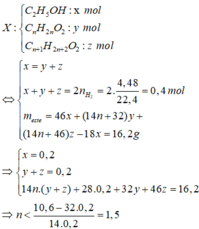
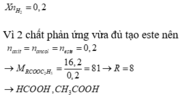
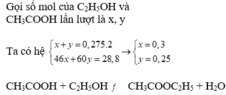

Chọn đáp án A
Đặt CTTQ của 2 axit là CnH2n+1COOH
Đặt số mol của ancol và axit trong X lần lượt là x, y
n H 2 = x + y 2 = 6 , 72 22 , 4 = 0 , 3 m o l
Các chất X trong phản ứng vừa đủ tạo este ⇒ x = y = 0 , 3 m o l
M ¯ e s t e = 25 0 , 3 = 83 , 33 ⇒ M ¯ a x i t = 83 , 33 + 18 - 32 = 69 , 33 ⇒ n = 5 3
Đốt cháy X: n H 2 O = 2 . 0 , 3 + 8 3 . 0 , 3 = 1 , 4 m o l
⇒ mbình tăng =18.1,4 = 25,2 g