Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi x, y lần lượt là số mol NO va NO2
\(\left\{{}\begin{matrix}x+y=0,3\left(mol\right)\\30x+46y=12,2\end{matrix}\right.\)
=> x= 0,1 (mol ) ; y=0,2 (mol)
\(n_{HNO_3}=4n_{NO}+2n_{NO_2}=4.0,1+2.0,2=0,8\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{NO}=x\left(mol\right)\\n_{NO_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{6,72}{22,4}=0,3\left(1\right)\)
Theo đề bài, có: 30x + 46y = 12,2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
Theo ĐLBT mol e, có: \(3n_{Fe}+2n_{Cu}=0,1.3+0,2=0,5\left(mol\right)\)
Muối thu được gồm: Fe(NO3)3 và Cu(NO3)2
BTNT Fe, Cu: nFe(NO3)3 = nFe và nCu(NO3)2 = nCu
BTNT N, có: nHNO3 = nNO + nNO2 + 3nFe(NO3)3 + 2nCu(NO3)2
= 0,1 + 0,2 + 0,5 = 0,8 (mol)
Bạn tham khảo nhé!





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

\(a,n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow n_{Al}=0,2(mol)\\ \Rightarrow m_{Al}=0,2.27=5,4(g)\\ b,m_{hh}=5,4+12,8=18,2(g)\\ c,n_{HCl}=0,6(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,3}=2M\)
a) \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
_____0,2<----0,6<---------------0,3
=> mAl = 0,2.27 = 5,4(g)
b) mhh = 5,4 + 12,8 = 18,2(g)
c) \(C_{M\left(HCl\right)}=\dfrac{0,6}{0,3}=2M\)

Tóm tắt:
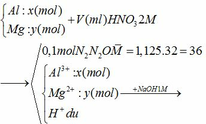
Gọi số mol của N2 và N2O lần lượt là
a và b (mol)
Ta có:
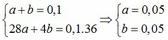


ne (KL nhường) = ne(N+5 nhận)
=> 2x + 3y = 0,5 + 0,4 (1)
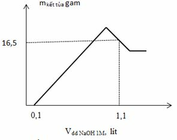
Từ đồ thị ta thấy tại giá trị V= 0,1 (lít) tức nNaOH = 0,1 (mol) mới bắt đầu xuất hiện kết tủa=> lượng NaOH này chính là lượng để trung hòa HNO3 dư sau phản ứng=> nHNO3 dư = nNaOH0,1 (mol) Ta thấy tại giá trị V= 1,1 (lít) tức nNaOH = 1,1 (lít) đồ thị đi lên cực đại sau đó lại đi xuống => kết tủa đạt cực đại sau đó bị hòa tan 1 phần ( chỉ có Al(OH)3 bị hoàn tan) Khi cho NaOH từ từ vào dung dich .Z xảy ra phản ứng:
H+ + OH- → H2O
0,1 → 0,1 (mol)
Mg2+ + 2OH- → Mg(OH)2↓
x → 2x (mol)
Al3+ + 3OH- → Al(OH)3↓
y → 3y →y (mol)
Al(OH)3↓ + OH- → AlO2- + 2H2O
(y – z ) → (y –z) (mol)
Gọi số mol của Al(OH)3 còn lại không bị hoàn tan là z (mol)
=> ta có: ∑ nNaOH = nH+dư + 2nMg2+ + 4nAl3+ - nAl(OH)3
=> 0,1 +2x + 4y – z = 1,1 (2)
Mặt khác: ∑ mkết tủa = mMg(OH)2 + mAl(OH)3 chưa hòa tan
=> 58x + 78z = 16,5 (3)
Từ (1), (2) và (3) => x = 0,2 ; y = 0,15 và z = 0,1 (mol)
=> m = mAl + mMg = 0,2.27 + 0,15.24 = 9 (g)
nHNO3 = nHNO3 dư + 2nN2 + 2nN2O + 3nAl(NO3)3 + 2nMg(NO3)2 = 0,1 + 2.0,05 + 2. 0,05 + 3.0,2 + 2.0,15 = 1,2 (mol)
=> VHNO3 = n : CM = 1,2 : 2 = 0,6 (lít) = 600 (ml)

\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right),n_{Al}=c\left(mol\right)\)
\(m_X=64a+56b+27b=35.7\left(g\right)\left(1\right)\)
\(n_{Cl_2}=\dfrac{21.84}{22.4}=0.975\left(mol\right)\)
\(Cu+Cl_2\underrightarrow{^{^{t^0}}}CuCl_2\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
\(Al+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}AlCl_3\)
\(n_{Cl_2}=a+1.5b+1.5c=0.975\left(mol\right)\left(2\right)\)
\(n_{hh}=ka+kb+kc=0.25\left(mol\right)\)
\(n_{H_2}=kb+k\cdot1.5c=0.2\left(mol\right)\)
\(\Leftrightarrow a-0.25b-0.875c=0\left(3\right)\)
\(\left(1\right),\left(2\right),\left(3\right):a=0.3,b=0.15,c=0.3\)
\(\%Cu=\dfrac{0.3\cdot64}{35.7}\cdot100\%=53.78\%\)
\(\%Fe=\dfrac{0.15\cdot56}{35.7}\cdot100\%=23.52\%\)
\(\text{%Al=22.7%}\)
Fe+6HNO3->Fe(NO3)3+3H20+3NO2
theodb 1 3
theo pt 0.02 0.06 (mol)
Al+6HNO3->Al(NO3)3+3H2O+3NO2
theo db 1 3
theo pt 0.04 0.12 (mol)
Cu+4HNO3->Cu(NO3)2+2H2O+2NO2
theo db 1 2
theo pt 0.03 0.06 (mol)
4Zn+10HNO3->3H2O+NH4NO3+4Zn(NO3)2
n N2O=0.06+0.06+0.12=0.24(mol)
->V=n:22.4=0.24:22.4=0.01(l)
ĐÁP SỐ: 0.01 l
mình hay làm sai lắm , có gì xin mọi người góp ý nha