Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Gọi thể tích dung dịch X là V (lít)
nNaOH = 1,5V
nKOH = V
nOH- = 1,5V+V = 2,5V
nH+ = nHCl + 2nH2SO4 = 0,2.0,1 + 2.0,2.0,2 = 0,1 mol
nOH- = nH+ => 2,5V = 0,1 => V = 0,04 lít = 40 ml

Chọn D
Trộn 3 dung dịch với thể tích bằng nhau thu được 150 ml dung dịch X → mỗi dung dịch lấy 50ml.
→ n H + = 0,05.0,2 + 0,05.2.0,1 + 0,05.0,08 = 0,024 mol.
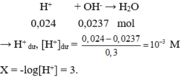

a) \([OH^-]=\left[KOH\right]=1,5M\)
b) Để trung hòa dung dịch A: \(n_{\left[OH^-\right]}=n_{\left[H^+\right]}\)
\(\Rightarrow0,15=0,5\cdot V_{HCl}\Rightarrow V_{HCl}=0,3l=300ml\)

a)
$KOH + HCl \to KCl + H_2O$
$n_{KOH} = 0,3(mol) < n_{HCl} = 1,05(mol)$ nên HCl dư
$n_{HCl\ dư} = 1,05 -0 ,3 = 0,75(mol)$
$n_{KCl} = n_{KOH} = 0,3(mol)$
$V_{dd} = 0,3+ 0,7 = 1(lít)$
Suy ra :
$[K^+] = \dfrac{0,3}{1} = 0,3M$
$[Cl^-] = \dfrac{0,75 + 0,3}{1} = 1,05M$
$[H^+] = \dfrac{0,75}{1} = 0,75M$
b)
$Ba(OH)_2 + 2HCl \to BaCl_2 + 2H_2O$
$n_{Ba(OH)_2} = \dfrac{1}{2}n_{HCl} = 0,375(mol)$
$V_{Ba(OH)_2} = \dfrac{0,375}{1,5} = 0,25(lít)$
\(n_{KOH}=0.3\cdot1=0.3\left(mol\right)\)
\(n_{HCl}=0.7\cdot1.5=1.05\left(mol\right)\)
\(KOH+HCl\rightarrow KCl+H_2O\)
\(0.3...........0.3..........0.3\)
Dung dịch D gồm : 0.3 (mol) KCl , 0.75 (mol) HCl dư
\(\left[K^+\right]=\dfrac{0.3}{0.3+0.7}=0.3\left(M\right)\)
\(\left[Cl^-\right]=\dfrac{0.3+0.75}{0.3+0.7}=1.05\left(M\right)\)
\(\left[H^+\right]=\dfrac{0.75}{0.3+0.7}=0.75\left(M\right)\)
\(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
\(0.375..................0.75\)
\(V_{dd_{Ba\left(OH\right)_2}}=\dfrac{0.375}{1.5}=0.25\left(l\right)\)

Đáp án D
VX = 0,3 lit
=> Thể tích mỗi dung dịch axit thành phần là 0,1 lit
=> nH+ = nHCl + 2nH2SO4 + 3nH3PO4 = 0,1.0,3 + 2.0,1.0,2 + 3.0,1.0,1 = 0,1 mol
Để trung hòa thì : nH+ = nOH- = 0,1 mol
Có : nOH- = nNaOH + 2nBa(OH)2 = (0,2 + 0,1.2).V.10-3 = 0,1 mol
=> V = 250 ml

Câu 1:
PT ion: \(H^++OH^-\rightarrow H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{OH^-}=0,6\cdot0,4+0,6\cdot0,3\cdot2=0,6\left(mol\right)\\n_{H^+}=0,2\cdot2,6=0,52\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\) H+ hết, OH- còn dư \(\Rightarrow n_{OH^-\left(dư\right)}=0,08\left(mol\right)\)
\(\Rightarrow\left[OH^-\right]=\dfrac{0,08}{0,6+0,2}=0,1\left(M\right)\) \(\Rightarrow pH=14+log\left(0,1\right)=13\)
Bài 2:
PT ion: \(H^++OH^-\rightarrow H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{OH^-}=0,3\cdot1,6=0,48\left(mol\right)\\n_{H^+}=0,2\cdot1\cdot2+0,2\cdot2=0,8\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\) OH- hết, H+ còn dư \(\Rightarrow n_{H^+\left(dư\right)}=0,32\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,32}{0,2+0,3}=0,64\left(M\right)\) \(\Rightarrow pH=-log\left(0,64\right)\approx0,19\)

Giải thích các bước giải:
pH = 9 → [H+] = 10−9(M)
[H+].[OH-]=10−14
→ [OH-] = 10−5(M)
→ nOH- = 10−5 . 1 = 10−5(mol)
pH=8 → [H+] = 10−8(M)
[H+].[OH-]=10−14
→ [OH-] = 10−6(M)
Gọi x lít là thể tích nước cần dùng
Ta có
\(\dfrac{10^{-5}}{x+1}\)= 10-6
→x=9
Chọn câu C.9 lít

Đáp án B