Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Sau phản ứng dung dịch chỉ chứa muối nitrat, chứng tỏ HNO3 đã hết. Do đó ta tính số mol electron Fe nhường theo mol H+ hoặc theo mol NO 3 - tham gia vào quá trình khử. Như vậy, vấn đề quan trọng nhất của bài tập này là tìm được sản phẩm khử


Đáp án A
Khi cho Al phản ứng với NaOH hoặc HCl thì số mol H2 thu được là như nhau:
nH2= 0,3 mol ⇒ nAl = 0,2 mol
Từ đó suy ra nH2 do Fe tạo ra = 0,4 - 0,3 = 0,1 mol
⇒nFe = 0,1 mol ⇒ nAl đã phản ứng tạo Fe là 0,1 mol vì:

⇒∑n Al trong X = 0,1 + 0,2 = 0,3mol

Đáp án C
Gọi a, b là số mol CuO và FexOy, viết sơ đồ phản ứng ta có:
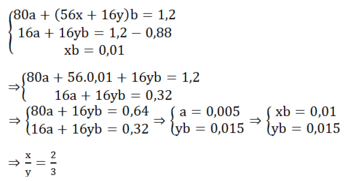

Đáp án C
Ta có: ![]()
suy ra số mol CO2 trong Z là 0,05 mol tức O bị khử 0,05 mol.
Gọi số mol Fe3O4 và CuO lần lượt là a, b
![]()
Cho Y tác dụng với 1,2 mol HNO3 thu được khí 0,175 mol khí NO2.
Bảo toàn N:
![]()
![]()
Ta có 2 TH xảy ra:
TH1: HNO3 dư.
![]()
![]()
TH2: HNO3 hết.
![]() nghiệm âm loại.
nghiệm âm loại.

Đáp án B
1-đúng, Cr bị thụ động.
2-sai, CrO3 là oxit axit.
3-đúng.
4-sai, Cr tác dụng với Cl2 tạo ra CrCl3.
5-đúng.
6-sai, Cr hoạt động mạnh hơn Fe.

Đáp án B
1-đúng, Cr bị thụ động.
2-sai, CrO3 là oxit axit.
3-đúng.
4-sai, Cr tác dụng với Cl2 tạo ra CrCl3.
5-đúng.
6-sai, Cr hoạt động mạnh hơn Fe.

Đáp án B
Do H2SO4 chưa biết nồng độ nên xét 2 trường hợp:
TH1: H2SO4 loãng:
Fe + H2SO4 → FeSO4 + H2
x y
⇒Loại vì x = y
TH2: H2SO4 đặc nóng
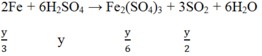
Ta có:
![]()
Do Fe dư nên tiếp tục xảy ra phản ứng:
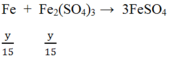
![]()
Vậy Fe hết
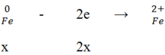
S + 2e → SO2
y y/2
Áp dụng định luật bảo toàn electron ta có: 2x = y
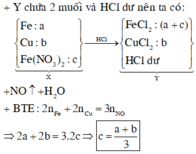
Đáp án cần chọn là: B