Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khi S phản ứng với các đơn chất có độ âm điện lớn hơn sẽ thể hiện tính khử
Do đó phản ứng (1) và (3), S đóng vai trò chất khử

Câu 28: Cho phương trình hóa học phản ứng: SO2 + H2SO4 ➜ 3S + 2H2O. Vai trò các chất tham gia phản ứng này là:
A. SO2 là chất oxi hóa, H2S là chất khử.
B. SO2 là chất khử, H2S là chất oxi hóa.
C. SO2 vừa là chất khử, vừa là chất oxi hóa.
D. H2S vừa là chất khử, vừa là chất oxi hóa.

a)H2S chỉ thể hiện tính khử vì số oxi hóa của S ở mức thấp nhất :-2 .(Không thể giảm nên chỉ có tình khử)
H2SO4 chỉ thể hiện tính oxi hóa vì số oxi hóa của S ở mức cao nhất :6 . (Không thể tăng nên chỉ có tính oxi hóa)
b)H2S + Pb(NO3)2-->PbS + 2HNO3
H2SO4+ FeS -->H2S + FeSO4

HD:
a)
Mg - 2e = Mg+2 (Sự oxi hóa, Mg là chất khử)
S+6 + 6e = S (Sự khử, H2SO4 là chất oxi hóa)
--------------------------
3Mg + S+6 = 3Mg+2 + S
3Mg + 4H2SO4 ---> 3MgSO4 + S + 4H2O
b)
2N-3 - 6e = N2 (Sự oxi hóa, NH3 là chất khử)
Cu+2 +2e = Cu (Sự khử, CuO là chất oxi hóa)
----------------------
2N-3 + 3Cu+2 = N2 + 3Cu
2NH3 + 3CuO ---> 3Cu + N2 + 3H2O

a. S---> SO 2 ---> KHSO 3 ---> SO 2
S+O2-to->SO2
SO2dư+KOh->KHSO3
KHSO3+HCl->KCl+H2O+SO2
b. FeS2--> SO2---> SO3---> H 2 SO4--->K 2 SO 4-->KCl ---> KNO 3
2FeS2+11\2O2-to->Fe2O3+4SO2
2SO2+O2-to->2SO3
SO3+H2O->H2SO4
H2SO4+2KOH->K2SO4+2H2O
K2SO4+BaCl2->2KCl+BaSO4
KCl+AgNO3->AgCl+KNO3
c. H 2 S ---> SO 2 ---> H 2 SO 4---> SO 2--->S
2H2S+3O2-to->2H2O+SO2
SO2+Br2+H2O->H2SO4+2HBr
H2SO4+Na2SO3->Na2SO4+H2O+SO2
SO2+2H2S->2H2O+3S

Giả sử: 1 gam C và Al
+ 1 gam C có 1/12 mol
1 mol C : ${\Delta _r},H_{298}^0$ = -393,5 kJ
1/12 mol C ${\Delta _r},H_{298}^0$ = -32,79 kJ
+ 1 gam Al có 1/27 mol
2 mol Al : ${\Delta _r},H_{298}^0$= -1675,7 kJ
1/27mol Al : ${\Delta _r},H_{298}^0$= -31,03 kJ
⇒ Với cùng một khối lượng C và Al, C khi đốt cháy tỏa ra nhiều nhiệt hơn.
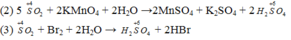
Đáp án D