Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)Gọi CTHH của oxit là \(R_xO_y\).
Trong phân tử có 5 nguyên tử tạo thành.
\(\Rightarrow x+y=5\left(1\right)\)
Theo bài: \(\%m_O=\dfrac{16y}{R\cdot a+16y}\cdot100\%=47,06\%\)
\(\Rightarrow\left\{{}\begin{matrix}a=2\\b=3\\R=27\Rightarrow Al\end{matrix}\right.\)
Vậy CTHH là \(Al_2O_3\) có tên nhôm oxit.
b)\(n_{Al_2O_3}=\dfrac{5,1}{102}=0,05mol\)
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
0,1 0,05
\(m_{Al\left(OH\right)_3}=0,1\cdot78=7,8g\)
\(H=80\%\Rightarrow m_{Al\left(OH\right)_3}=7,8\cdot80\%=6,24g\)
a) Đặt CTHH của oxit là NxOy
Theo đề bài ta có : x + y = 5(1)
Mà : %O=\(\dfrac{16y}{Nx+16y}100=47,06\%\)=47,06%(2)
Giai hệ phương trình (1) và (2) ta có :
x=2,y=3,N=27g\mol
⇒CTHH:Al2O3.
Gọi tên : Nhôm oxit .
b)
PT 2Al(0H)3-to>Al2O3+3H2O
nAl2O3=0,05mol
=> nAl(OH)3 =0,1mol
mà H = 80% nên nAl(OH)3=0,125mol
=> mAl(OH)3 cần dùng = 0,125.78=9,75g

Đặt công thức oxit là RaOb
Theo đề ra, ta có: a + b = 5 (1)
Mặt khác: %mO = \(\frac{16b}{Ra+16b}\times100\%=47,06\%\) (2)
Giải hệ (1), (2) ta được \(\left\{\begin{matrix}a=2\\b=3\\R=27\left(\frac{g}{mol}\right)\end{matrix}\right.\)
=> CTHH của oxit là Al2O3
Gọi tên: Nhôm Oxit

1)
PTKR2Ox = 2.NTKR + 16x = 102 (đvC)
| x | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| NTKR | 43(Loại) | 35(Loại) | 27(Al) | 19(Loại) | 11(Loại) | 3(Loại) | Loại | Loại |
=> R là Al
2)
CTHH: RxOy
\(\%R=\dfrac{x.NTK_R}{160}.100\%=70\%\)
=> \(NTK_R=\dfrac{112}{x}\left(đvC\right)\)
Chỉ có x = 2 thỏa mãn \(NTK_R=\dfrac{112}{2}=56\left(đvC\right)\)
=> R là Fe
PTKFe2Oy = 160 (đvC)
=> y = 3
CTHH: Fe2O3

a) Đặt công thức oxit chung là MxOy
Theo đề bài ra , ta có : x + y = 5
Mặt khác : %O = 47,06% \(\Rightarrow\) %M = 52,94%
Mà : \(\dfrac{16y}{Mx}=\dfrac{47,06}{52,94}\)
Lập bảng giá trị :
| x | 1 | 2 | 3 | 4 |
| y | 4 | 3 | 2 | 1 |
| M | 72 | 27 | 12 |
4,5 |
Nghiệm phù hợp khi x = 2 ; M = 27 \(\Rightarrow\) M là Al
Vậy công thức oxit là Al2O3
b)
2Al(OH)3 \(\rightarrow\) Al2O3 + 3H2O ( 1 )
a---------------\(\dfrac{a}{2}\)
Ta có : \(n_{Al_2O_3}=\dfrac{m}{M}=\dfrac{5,1}{102}=0,05\left(mol\right)\)
Từ ( 1 ) \(\Rightarrow n_{Al\left(OH\right)_3}=0,1\left(mol\right)\)
Vì H = 80% nên \(n_{Al\left(OH\right)_3}\) cần dùng là :
\(n_{Al\left(OH\right)_3}=\dfrac{0,1\cdot100}{80}=0,125\left(mol\right)\)
\(\Rightarrow m_{Al\left(OH\right)_3}=0,125\cdot78=9,75\left(g\right)\)
Vậy cần 9,75 gam Al(OH)3
LÀM LẠI CÂU B QUÊN CÂN BẰNG PTHH:
PT 2Al(0H)3->Al2O3+3H2O
nAl2O3=0,05mol
=> nAl(OH)3 =0,1mol
mà H = 80% nên nAl(OH)3=0,125mol
=> mAl(OH)3 cần dùng = 0,125.78=9,75g
Vậy..........................

a) Câu hỏi của Trần Thị Thùy Trang - Hóa học lớp 8 | Học trực tuyến
b) Ta có: Hiệu suất 80% thì tạo thành 5,1g Al2O3
.....Vậy: Hiệu suất 100% thì tạo thành m (g) Al2O3
=> m = \(\dfrac{100\times5,1}{80}=6,375\left(g\right)\)
=> nAl2O3 = \(\dfrac{6,375}{102}=0,0625\) mol
Pt: 2Al(OH)3 --to--> Al2O3 + 3H2O
....0,125 mol<-------0,0625 mol
mAl(OH)3 = 0,125 . 78 = 9,75 (g)
Vậy .........................

\(m_O=\frac{47,06.102}{100}=48g\)
\(\rightarrow a=n_O=\frac{48}{16}=3mol\)
Có \(M_R.2+M_O.3=102\)
\(\rightarrow M_R.2+16.3=102\)
\(\rightarrow M_R=\frac{102-16.3}{2}=27g/mol\)
CT của Oxit X là \(Al_2O_3\)
\(m_O=\frac{47,06\cdot102}{100}=48g\)
\(\rightarrow a=n_O=\frac{48}{16}=3mol\)
\(M_R\cdot2+M_O\cdot3=102\)
\(\Leftrightarrow M_R\cdot2+16\cdot3=102\)
\(\rightarrow M_R=\frac{102-16\cdot3}{2}=\frac{27g}{mol}\)
Công thức của oxit X là \(Al_2O_3\)

Gọi công thức tổng quát là $XH_4$
\(\%H=25\%\\ \Rightarrow \dfrac{4}{X+4}.100\%=25\%\\ \Rightarrow X=12\\ Tên:\ Cacbon\\ CTHH:\ CH_4\)

1.\(\dfrac{m_{Al}}{m_O}=\dfrac{9}{8}\)
\(Al_xO_y\)
\(x:y=\dfrac{9}{27}:\dfrac{8}{16}=\dfrac{1}{3}:\dfrac{1}{2}=2:3\)
Vậy CTHH là \(Al_2O_3\)
2.\(\rightarrow\%S=100-60=40\%\)
\(S_xO_y\)
\(x:y=\dfrac{40}{32}:\dfrac{60}{16}=1,25:3,75=1:3\)
Vậy CTHH là \(SO_3\)
3.
a.b.
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_{H_2SO_4}=2.0,2=0,4mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 < 0,4 ( mol )
0,2 0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
Chất dư là H2SO4
\(m_{H_2SO_4\left(dư\right)}=\left(0,4-0,2\right).98=19,6g\)
c.Nồng độ gì bạn nhỉ?

Giả sử khối lượng oxit là 10g ⇒ m F e = 7g ; m O = 3g
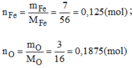
Vậy: 0,125 mol nguyên tử Fe kết hợp với 0,1875 mol nguyên tử O.
Suy ra 2 mol nguyên tử Fe kết hợp với 3 mol nguyên tử O (vì số nguyên tử luôn là số nguyên).
→ Công thức hóa học đơn giản của oxit sắt là: F e 2 O 3
Câu hỏi của Trần Thị Thùy Trang - Hóa học lớp 8 | Học trực tuyến
Hệ đó giải kiểu j vậy nhở???