Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Thêm một lượng dung dịch HCl bốc khói vào dung dịch HCl 2M làm tăng nồng độ chất phản ứng HCl → tốc độ phản ứng tăng
Đun nóng hỗn hợp phản ứng, tăng nhiệt độ làm tăng tốc độ phản ứng
Tăng thể tích dung dịch lên gấp đôi, nồng độ không đổi → tốc độ phản ứng không ảnh hưởng
Thay CaCO3 dạng hạt bằng CaCO3 dạng bột → tăng diện tích tiếp xúc tăng tốc độ phản ứng.
Tăng áp suất của bình phản ứng, vì phản ứng không có sự tham gia của chất khí→tăng áp suất không ảnh hưởng đến tốc độ
Vậy có 3 yếu tố làm tăng tốc độ phản ứng. Đáp án B.

Các yếu tố làm tăng tốc độ phản ứng là: nhiệt độ (tăng thì tđpu tăng), áp suất (tăng thì tốc độ
phản ứng có chất khí tăng), S tiếp xúc (tăng thì tốc độ phản ứng tăng), nồng độ (tăng thì tốc độ phản ứng
tăng), xúc tác (luôn tăng)
(a) Có làm tăng tốc độ vì tăng diện tích tiếp xúc của oxi với Cu (ở ngoài không khí còn nhiều khí khác
chiếm chỗ)
(b) Đúng do làm tăng diện tích tiếp xúc giữa Zn và axit
(c) Có làm tăng vì phản ứng có chất khí, tốc độ phản ứng tăng khi tăng áp suất
(d) Không làm thay đổi vì nồng độ của HCl không thay đổi nên tốc độ phản ứng không tăng
Có 3 thay đổi làm tăng tốc độ phản ứng. Đáp án C

a) Tốc độ phản ứng tăng lên (tăng diện tích bề mặt).
b) Tốc độ phản ứng giảm xuống (giảm nồng độ chất phản ứng).
c) Tốc độ phản ứng tăng.
d) Tốc độ phản ứng không thay đổi.

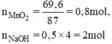
a) Phương trình hóa học của phản ứng:
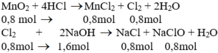
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 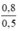 = 1,6 mol/ lit
= 1,6 mol/ lit
CM (NaOH)dư = 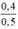 = 0,8 mol/ lit
= 0,8 mol/ lit

\(n_{MnO_2} = \dfrac{4,35}{87} = 0,05(mol)\)
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,05..................................0,05..................(mol)
\(n_{NaOH} = 0,3.0,1 = 0,03(mol)\)
2NaOH + Cl2 → NaCl + NaClO + H2O
0,03........0,05.....0,015.......0,015....................(mol)
Vậy :
\(C_{M_{NaCl}} = C_{M_{NaClO}} = \dfrac{0,015}{0,3} = 0,05M\)

(1), (2) Thay a gam Fe hạt thành a gam Fe bột hoặc dạng lá → làm tăng diện tích tiếp xúc của
Fe với H2SO4 → làm tăng tốc độ
(3) 0,5 M < b → làm giảm nồng độ của H2SO4 → làm giảm tốc độ phản ứng
(4) Tăng thể tích H2SO4 làm giảm nồng độ H2SO4 →tốc độ phản ứng giảm
(5) Tăng gấp đôi nồng độ phản ứng → tốc độ phản ứng tăng
(6) Tăng nhiệt độ tốc độ phản ứng tăng
Vậy có 4 yếu tố làm tăng tốc độ phản ứng. Đáp án C.

a) Khi thay a g hạt Zn = a g bột Zn
=> Chất tham gia được nghiền nhỏ
=> Diện tích bề mặt tiếp xúc của Zn với HCl tăng
=> Tốc độ phản ứng tăng
=> Khí thoát ra nhanh hơn
b) Khi thay dung dịch HCl 2 M = dung dịch HCl 1 M
=> Nồng độ chất tham gia giảm
=> Tốc độ phản ứng giảm
=> Khí thoát ra chậm hơn
c) Khi đun nóng nhẹ dung dịch HCl
=> Nhiệt độ của phản ứng tăng
=> Tốc độ phản ứng tăng
=> Khí thoát ra nhanh hơn