Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Gọi công thức chung của hai muối cacbonat kim loại hóa trị II là RCO3
RCO3 → RO + CO2
Áp dụng định luật bảo toàn khối lượng ta có:
mCO2 = mRCO3 - mRO = 13,4 - 6,8 = 6,6 (g)
⇒ nCO2 = 0,15 mol
Ta có: nNaOH = 0,075 mol
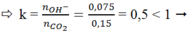
ð tạo ra muối NaHCO3 và CO2 dư.
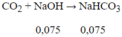
⇒mmuối = 0,075.84 = 6,3(g)

Đáp án B
Ta có:
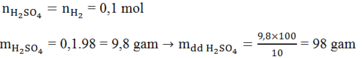
Áp dụng định luật bảo toàn khôi lượng:
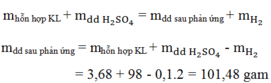

Đáp án D
Khối lượng Fe = 0,3m gam và khối lượng Cu = 0,7m gam
Sau phản ứng còn 0,75m gam → Fe chỉ phản ứng 0,25m gam; Fe dư vậy sau phản ứng chỉ thu được muối Fe2+.
Ta có:
![]()
Số mol của Fe(NO3)2 = 0,25m/56
Sơ đồ phản ứng:
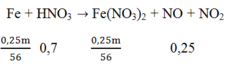
Áp dụng ĐLBT nguyên tố N ta có:
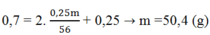

Đáp án B
Zn có tính khử mạnh hơn Fe, Zn sẽ phản ứng với dung dịch CuSO4 trước.
Theo đề: hỗn hợp rắn Z phản ứng với dung dịch H2SO4 loãng thu được 1 muối duy nhất → trong hỗn hợp rắn Z có Cu và Fe dư. Vậy mFe dư = 0,28 (g) và mCu = 2,84 - 0,28 = 2,56 (g)
Ta có: khối lượng hỗn hợp X phản ứng với Cu2+ = 2,7 - 0,28 = 2,42 (g)
Gọi nZn = x mol; nFe pư = y mol
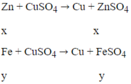
Ta có hệ:
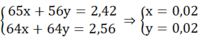
mFe ban đầu = 0,02.56 + 0,28 = 1,4 (g)
![]()

Đáp án B
Ta có:
![]()
mCu = 0,7m (g)
Vì Fe phản ứng trước Cu và sau khi phản ứng còn 0,75m (g) chất rắn → Cu chưa phản ứng 0,7m
Fe dư 0,75m - 0,7m = 0,05m → mFe pư = 0,2m - 0,05m = 0,25m (g)
Fe dư → Chỉ tạo muối Fe(NO3)2
HNO3 hết (Lưu ý chỉ H+ hết, NO3- còn trong muối).
Quá trình nhường electron:

Quá trình nhận electron:
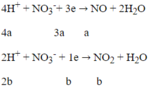
Áp dụng định luật bảo toàn electron:
![]()
→ m = 50,4

Chọn A.
Ta có: n Y = n X = 0 , 0555 m o l v à n K O H = 0 , 065 m o l Þ Y chứa este đơn chức (0,045 mol) và este hai chức (0,01 mol) (Vì các muối có mạch không nhánh nên tối đa 2 chức).
Đốt 0,055 mol X cần n O 2 = 0 , 055 . 0 , 5 0 , 1 = 0 , 275 m o l
Khi đốt Y, gọi CO2 (u mol) và H2O (v mol)
![]() Þ u = 0,245 mol và v = 0,235 mol
Þ u = 0,245 mol và v = 0,235 mol
T chứa C (a mol), H (b mol) và O (0,065 mol)
Khi đó: 
n C (muối) = u-a= 0,085 và → B T H n H (muối) = 2 v + n K O H - b = 0 , 085
Do nC (muối) = nH (muối) nên các muối có số C = số H.
Þ Muối gồm 

Chọn A.
Ta có: n Y = n H 2 = 0 , 04 m o l mol
=> E gồm các este của ancol (0,04) và các este của phenol (0,08 – 0,04 = 0,04)
mà n H 2 O = n este của phenol = 0,04 mol và n K O H = n este của ancol + 2neste của phenol = 0,12 mol
→ B T K L m E + m K O H = m muối + m ancol + m H 2 O Þ m muối = 13,7 gam

ta có:\(n_{AlCl2}=33,6:22,4=1,5\left(mol\right)\)
PTHH: \(2Al+6HCl\rightarrow2AlCl_{2_{ }}+3H_2\)
ban đầu: 0,1 1,5(mol)
phản ứng: 0,1\(\rightarrow\) 0,1 (mol)
sau pư: \(\frac{1}{30}\) 0 1,4(mol)
vậy sau pư HCl hết, AlCl2 dư
mAl= \(\frac{1}{30}.27=0,9\left(g\right)\)
chúc bạn học tốt like nha![]()

Đáp án C
Ta có: ![]()
suy ra số mol CO2 trong Z là 0,05 mol tức O bị khử 0,05 mol.
Gọi số mol Fe3O4 và CuO lần lượt là a, b
![]()
Cho Y tác dụng với 1,2 mol HNO3 thu được khí 0,175 mol khí NO2.
Bảo toàn N:
![]()
![]()
Ta có 2 TH xảy ra:
TH1: HNO3 dư.
![]()
![]()
TH2: HNO3 hết.
![]() nghiệm âm loại.
nghiệm âm loại.
này lớp 9 nhe mọi người ... mọi người giúp mình với