
![]()

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

![]()
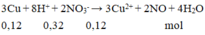


nCu= 0,12 mol; nHNO3= 0,12 mol; nH2SO4= 0,1 mol
3Cuhết + 8H+hết + 2NO3-dư® 3Cu2+ + 2NO + 4H2O
0,12 0,32 0,12 ® 0,12
nNO3- dư= 0,12- 0,12.2/3= 0,04 mol
Muối khan thu được có chứa: 0,12 mol Cu2+, 0,04 mol NO3- và 0,1 mol SO42-
→ m muối khan= 0,12.64+ 0,04.62+ 0,1.96= 19,76 gam

Cho 0,87 gam hỗn hợp gồm Fe, Cu và Al vào dung dịch H2SO4
→ Chất rắn không tan là Cu, mCu= 0,32 gam, nCu=0,005 mol
2Al+ 3H2SO4 → Al2(SO4)3+ 3H2
Fe+ H2SO4 → FeSO4+ H2
Ta có mFe + mAl = 0,87 - 0,32 = 0,55 gam
Đặt nFe= x mol, nAl= y mol → 56x + 27y= 0,55
nH2= 1,5.x+ y= 0,448/22,4= 0,02 mol
=> x = 0,005; y= 0,01
ta có nH2SO4 ban đầu= 0,3.0,1=0,03 mol, nH2= 0,448/22,4=0,02 mol
nH+ còn lại = nH+ ban đầu- nH+ pứ= 2.nH2SO4- 2.nH2= 2. 0,03- 2.0,02= 0,02 mol
nNO3- =nNaNO3= 0,005 mol
Ta có các bán phản ứng sau
Fe2+ → Fe3+ + 1e
0,005 0,005
Cu -→ Cu2+ + 2e
0,005 0,01
=> ne cho = 0,015 mol= n e nhận
4H+ + NO3- + 3e → NO + 2H2O (3)
0,02 0,005 0,015 0,005
V = 0,005.22,4 = 0,112 lít
Theo bán phản ứng (3) thì cả H+ và NO3- đều hết
Khối lượng muối=Khối lượng kim loại + mNa+ + mSO4
= 0,87 + 0,005.23 + 0,03.96 = 3,865 gam
Đáp án D

nNO = 0,15 (mol)
Gọi a là số mol Cu trong X đã phản ứng. Gọi b là số mol Fe3O4 trong X
Ta có: 64a + 232b = 61,2 – 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo bảo toàn e: 2a + 2.3b – 2.4b = 3.0,15
Từ đó: a = 0,375; b = 0,15
Muối khan gồm có: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
mmuối = 188.0,375 + 180.0,45 = 151,5 (gam)
Đáp án B

Ta có: nFe=0,02 mol; nCu= 0,03 mol, nH2SO4= 0,2 mol, nNaNO3= 0,08 mol
nH+= 2n H 2 S O 4 = 0,4 mol, n N O 3 -= 0,08 mol
3Cu + 8H+ + 2NO3-® 3Cu2+ + 2NO + 4H2O (1)
0,03 0,08 0,02 ® 0,03 mol
Fe + 4H+ + NO3- ® Fe3+ + NO + 2H2O (2)
0,02 0,08 0,02 ® 0,02 mol
Tổng số mol H+ tham gia phản ứng (1) và (2) là 0,08+ 0,08= 0,16 mol
→nH+ dư= 0,4-0,16= 0,24 mol
Dung dịch X có chứa Cu2+, Fe3+ và H+
H++ OH-→H2O (3)
Cu2++ 2OH- → Cu(OH)2 (4)
Fe3++ 3OH- → Fe(OH)3 (5)
Theo PT (3), (4), (5) ta có
nOH-= nH++ 2nCu2++ 3nFe3+= 0,24+ 2.0,03+ 3.0,02= 0,36 mol= nNaOH
→V= 0,36 lít= 360 ml
Đáp án A

Đáp án A
mMg pư = 8,64 – 4,08 = 4,56 (g) => nMg pư = 0,19 (mol) => ne (Mg nhường) = 0,38 (mol)
nX = 0,08 (mol) => MX = 1,84: 0,08 = 23(g/mol) => khí X là H2
Gọi nNO = a (mol); nH2 = b (mol)
∑ nX = a + b = 0,08 (1)
∑ mX = 30a + 2b = 1,84 (2)
Từ (1) và (2) => a = 0,06 ; b = 0,02
=> ∑ ne (nhận) = 3nNO + 2nH2 = 0,06.3 + 0,02.2 = 0,22 < ne (Mg nhường) = 0,38
=> tạo muối NH4+
Bảo toàn electron => 2nMg pư = 3nNO + 2nH2 + 8nNH4+
=> nNH4+ = (2nMg pư - 3nNO - 2nH2)/8 = 0,02 (mol)
BTNT N => nNO3- = nNO + nNH4+ = 0,06 + 0,02 = 0,08 (mol) => nNa+ = 0,08 (mol)
=> mmuối = mMgSO4 + m(NH4)2SO4 + mNa2SO4
= 0,19. 120 + 132. 0,01 + 0,04. 142
= 29,8 (g) ≈ 29,6 (g)

Đáp án A
nOH- = 0,375 mol, nH3PO4 = 0,2 mol
Có T = nOH-/ nH3PO4 = 0,375/0,2 = 1,875
Nên sau phản ứng thu được 2 loại muối là H2PO4- và HPO42-
H3PO4+ OH- → H2PO4-+ H2O
x mol x x mol
H3PO4+ 2OH-→ HPO42-+ 2H2O
y mol 2y y mol
Ta có x+y = 0,2; x+2y = 0,375 nên x = 0,025 mol; y = 0,175 mol
Dung dịch X có Na+: 0,125 mol; Ba2+: 0,125mol; H2PO4-: 0,025mol; HPO42-: 0,175 mol
Khối lượng muối khi cô cạn là
0,125.23+ 0,125.137+ 0,025.97+ 0,175.96 = 39,225 gam