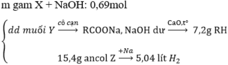Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3) đầu tiên bạn viết PTHH đi:Na2CO3 + 2HCL - 2NaCl + H2O + Co2
nNa2CO3=1.886mol
nHCL=3.287mol
chú ý nha số ko dc chẳng nên mình lấy đến phần nghìn nhé!
Bạn suy ra dc số Na2CO3 dư, tính theo số mol HCl
mNaCL=192.2895g
m Na2Co3 (dư)=25.705g
khối lượng dd:200+120=320g
C% củ từng chất:Na2Co3=8%
NaCl=60%
Gọi côg thức hoá học của oxit Kim loại hoá trị 3 là X2O3
X2O3 + 3H2SO4 -----------> X2(SO4)3 + 3H2O
Khối lượng dd X2(SO4)3 sau PƯ là
m(dd)X2(SO4)3 = 10,2 + 331,8 = 342 (g)
Khối lượng chất tan X2(SO4)3 sau PƯ là
m(ct>X2(SO4)3 = 342 . 10 : 100 = 34,2 (g)
Theo pt PƯ : nX2O3 = nX2(SO4)3
=> 10,2 trên (2Mx+48) = 34,2 trên (2Mx + 288)
=> 34,2 .( 2Mx + 48 ) = 10,2 .(2Mx +288)
=> 68,4Mx + 1641,6 = 20,4Mx + 2937,6
=> 48Mx = 1296
=> Mx = 27
Do đó kim loại X là Al
Côg thức hoá học của oxit kim loại là Al2O3
b, Số mol của Al2O3 là
nAl2O3 = 10,2 : 102 = 0,1 (mol)
Theo pt PƯ nAl2O3 = 3nH2SO4
=>nH2SO4 = 0,3 (mol)
Khối lượng của H2SO4
mH2SO4 = 0,3 . 98 = 29,4 (g)
Phần trăm dung dịch của axit H2SO4
C%(dd)H2SO4 = 29,4 : 331,8 .100% ~ 8.87%

Đáp án : A
nH2 = 0,1 mol => n ancol = 2nH2 = 0,2 mol (vì ancol đơn chức)
=> M ancol = 9 , 2 0 , 2 = 46 (C2H5OH)
Đun 0,1 mol X tạo ra 0,2 mol ancol => X là este 2 chức, muối của Y là muối 2 chức NaOOCRCOONa
Theo đề bài: 0,1.(R + 67.2) = 13,4 => R = 0
=> X là C2H5OOCCOOC2H5 (đietyl oxalat)

Đáp án C
Lời giải : số mol của Fe :0,2 mol
Ta có Fe + 2HCl → FeCl2 + H2
Thì số mol của H2 : 0,2 mol nên V=4,48 lít

\(n_{Mg}=x;n_{Fe}=y\\ PTHH:Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ hpt:\left\{{}\begin{matrix}24x+56y=8\\22,4\left(x+y\right)=4,48\end{matrix}\right.\Leftrightarrow x=y=0,1\\ \rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\frac{0,1.24}{8}.100\%=30\%\\\%m_{Fe}=100-30=70\%\end{matrix}\right.\\ C\%_{H_2SO_4}=\frac{98.\left(0,1+0,1\right)}{200}.100\%=9,8\left(\%\right)\\ m_M=0,1.\left(120+152\right)=27,2\left(g\right)\)
a) Mg +H2SO4----->MgSO4 +H2
x------------x--------------x---------x
b) Fe +H2SO4----->FeSO4 +H2
y----------y-------------y---------y
Gọi n\(_{Mg}=x\Rightarrow m_{_{ }Mg}=24x\)
\(n_{Fe}=y\Rightarrow m_{Fe}=56y\)
=> 24x +56y=8(1)
Mặt khác
n\(_{H2}=\frac{4,48}{22,4}=0,2mol\)
=> x+y=0,2(2)
Từ 1 và 2 ta có hệ pt
\(\left\{{}\begin{matrix}24x+56y=8\\x+y=0,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\)
%m\(_{Mg}=\frac{0,1.24}{8}.100\%=30\%\)
%m\(_{Fe}=100\%-30\%=70\%\)
b) Theo pthh
n\(_{H2SO4}=n_{_{ }H2}=0,2mol\)
C%=\(\frac{0,2.98}{200}.100\%=\)9,8%
c) m \(_{muối}=0,1\left(120+152\right)=\)27,2(g)
Nhớ tích cho mình nhé