

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





| CHÚ Ý |
| + Với các bài toán liên quan tới tính oxi hóa của trong môi trường H+ thì khi có khí H2 bay ra → toàn bộ N trong phải chuyển hết vào các sản phẩm khử. + Liên qua tới Fe thì khi có khí H2 thoát ra dung dịch vẫn có thể chứa hỗn hợp muối Fe2+ và Fe3+. |

Đáp án B
Gọi a, b và c lần lượt là số mol của Mg, Fe3O4 và Fe(NO3)2.
Hỗn hợp khí Y gồm NO (0,07 mol) và H2 (0,03 mol).
Cho 8,66 gam X tác dụng với dung dịch hỗn hợp HCl và HNO3 thì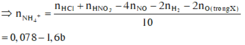
Cho Y tác dụng với NaOH, lọc kết tủa đun nóng thu được 10,4 gam hỗn hợp rắn gồm MgO (a mol) và Fe2O3 (1,5b + 0,5c) mol. Từ dữ kiện đề bài ta có hệ sau
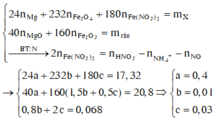

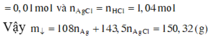

Đáp án A
Mg + (Cu(NO3)2, H2SO4). Ta thấy:
+) Tạo hỗn hợp 2 kim loại => Cu, Mg dư
+) Tạo hỗn hợp 2 khí có M = 8.2 = 16 g/mol. 1 khí hóa nâu ngoài không khí => NO (M = 30)
=> Khí còn lại phải có M < 16 => H2 => H+ dư hơn so với NO3-.
- nY = 0,896: 22,4 = 0,04 mol = nNO + nH2
Và: mY = mNO + mH2 = 30nNO + 2nH2 = 16.0,04 = 0,64
=> nNO = nH2 = 0,02 mol
- Thứ tự phản ứng sẽ là:
Mg + H+ + NO3-
Mg + Cu2+
Mg + H+
- Gọi số mol Cu2+ phản ứng là x => nCu = x = nMg dư
=> mCu + mMg dư = 1,76g = 64x + 24x => x = 0,02 mol
nMg bđ = 4,08: 24 = 0,17 mol => nMg pứ = 0,17 – 0,02 = 0,15 mol
Giả sử có NH4+ trong dung dịch X
=> Bảo toàn Nito: 2nCu(NO3)2 = nNO + nNH4 => nNH4 = 2.0,02 – 0,02 = 0,02 mol
=> Trong dung dịch X có 0,15 mol MgSO4 và 0,01 mol (NH4)2SO4
=> mmuối = 0,15.120 + 0,01.132 = 19,32g (Gần nhất với giá trị 19,5g)

Đáp án A
+ M ¯ Y = 16 Y c h ứ a N O ( h ó a n â u ) ⇒ Y c ó N O : x H 2 : y ⇒ x + y = 0 , 04 30 x + 2 y = 0 , 04 . 16 ⇒ x = 0 , 02 y = 0 , 02 + K i m l o ạ i g ồ m M g d ư , C u , n M g d ư = n C u = 1 , 76 64 + 24 = 0 , 02 m o l . + S ơ đ ồ p h ả n ứ n g : M g ⏟ m ( g ) + H 2 S O 4 C u ( N O 3 ) 2 → N O : 0 , 02 H 2 : 0 , 02 M g 2 + S O 4 2 - N H 4 + C u : 0 , 02 M g d ư : 0 , 02 + B T N T C u : n C u ( N O 3 ) 2 = n C u = 0 , 02 B T N T N : n N H 4 + = 2 n C u ( N O 3 ) 2 - n N O = 0 , 02 B T E : 2 n M g p ư = 3 n N O + 2 n H 2 + 8 n N H 4 + + 2 n C u 2 + ⇒ n M g p ư = 0 , 15 m = 4 , 08