

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Chọn B
Bảo toàn electron:
ne kim loại nhường = 4nO2 + 2nH2 = 4. 0,08 + 2.0,14 = 0,6 (mol)
=> dd Z chứa nOH- = 0,6 (mol)
Dd Z tác dụng với NaHCO3 dư => nBa2+ = nBaCO3 = 0,2 (mol)
Dd Z tác dụng với 0,45 mol CO2 => thu được nCO32- = 0,15 ; nHCO3- = 0,3 (mol)
=> mBaCO3 ↓ = 0,15.197 = 29,55 (g) ( Tính theo số mol của CO32-)

Đáp án B
Gọi a, b và c lần lượt là số mol của Mg, Fe3O4 và Fe(NO3)2.
Hỗn hợp khí Y gồm NO (0,07 mol) và H2 (0,03 mol).
Cho 8,66 gam X tác dụng với dung dịch hỗn hợp HCl và HNO3 thì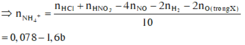
Cho Y tác dụng với NaOH, lọc kết tủa đun nóng thu được 10,4 gam hỗn hợp rắn gồm MgO (a mol) và Fe2O3 (1,5b + 0,5c) mol. Từ dữ kiện đề bài ta có hệ sau
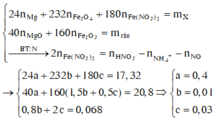

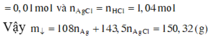

Đáp án B
Giải:
Phần 1: có H2 thoát ra => Al dư . nAl dư = 2/3 nH2 = 0,03
Chất rắn không tan là Fe , nFe = 0,09 => tỉ lệ mol Al và Fe là 1:3 Phần 2 : Đặt nAl=a , nFe=b
Ta có : 3a=b , 3a+3b=3nNO= 1,08 => a=0,09 ; b=0,27 => nAl2O3 = 0,12
Tỉ lệ mol của Al và Al2O3 là 3:4 => nAl2O3 trong phần 1 = 4/3 nAl=0,04
Vậy m = mAl + mFe + mAl2O3 = 0,03.27+0,04.102+5,04+29,79=39,72g
nFe = 0,09 ; nO=3 nAl2O3=0,12 => nFe:nO=3/4 => oxit sắt là Fe3O4

Đáp án B
nOH- = 2nH2 = 0,4
nCl- = 2nH2 = 0,3
m↓ = 5,2 + 0,3.17 = 10,3 g
mmuối = 5,2+0,3.35,5= 15,85 g