Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Fe+H_2SO_4 \to FeSO_4+H_2\\ n_{H_2}=0,15(mol)\\ a/\\ n_{Fe}=n_{H_2}=0,15(mol)\\ m_{Fe}=0,15.56=8,4(g)\\ b/\\ n_{H_2SO_4}=n_{H_2}=0,15(mol)\\ CM_{H_2SO_4}=\dfrac{0,15}{2}=0,75M c/\\ n_{FeSO_4}=n_{H_2}=0,15(mol)\\ CM_{FeSO_4}=\dfrac{0,15}{0,2}=0,75M\\\)

\(a.n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ Ba\left(OH\right)_2+SO_2\rightarrow BaSO_3\downarrow+H_2O\\ n_{BaSO_3}=n_{Ba\left(OH\right)_2}=n_{SO_2}=0,3\left(mol\right)\\ m_{BaSO_3}=217.0,3=65,1\left(g\right)\\ b.C_{MddBa\left(OH\right)_2}=\dfrac{0,3}{0,2}=1,5\left(M\right)\)

Ta có: \(n_{Fe}=\dfrac{3,92}{56}=0,07\left(mol\right)\)
\(PTHH:Fe+CuSO_4--->FeSO_4+Cu\downarrow\)
a. Theo PT: \(n_{Cu}=n_{FeSO_4}=n_{Fe}=0,07\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,07.64=4,48\left(g\right)\)
Ta có: \(V_{dd_{FeSO_4}}=V_{dd_{CuSO_4}}=\dfrac{200}{1000}=0,2\left(lít\right)\)
\(\Rightarrow C_{M_{FeSO_4}}=\dfrac{0,07}{0,2}=0,35M\)

a,\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: 0,1 0,1 0,1 0,1
b,\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c,\(C_{M_{ddH_2SO_4}}=\dfrac{0,1}{0,2}=0,5M\)
d,\(C_{M_{ddFeSO_4}}=\dfrac{0,1}{0,2}=0,5M\)

a) \(n_{NaOH}=0,2.1=0,2\left(mol\right);n_{H_2SO_4}=0,15.2=0,3\left(mol\right)\)
PTHH: 2NaOH + H2SO4 → Na2SO4 + 2H2O
Mol: 0,2 0,1
Ta có: \(\dfrac{0,2}{2}< \dfrac{0,3}{1}\) ⇒ NaOH hết, H2SO4 dư
\(m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
b) Vdd sau pứ = 0,2 + 0,15 = 0,35 (l)
\(C_{M_{ddNa_2SO_4}}=\dfrac{0,1}{0,35}=\dfrac{2}{7}\approx0,2857M\)
\(C_{M_{ddH_2SO_4dư}}=\dfrac{0,3-0,1}{0,35}=\dfrac{4}{7}\approx0,57M\)
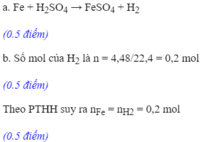

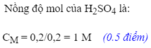
a)
$Fe + H_2SO_4 \to FeSO_4 + H_2$
Ta thấy : $n_{Fe} = \dfrac{5,6}{56} = 0,1 < n_{H_2SO_4} = 0,1.0,2 = 0,02$ nên Fe dư
$n_{FeSO_4} = n_{H_2SO_4} = 0,02(mol)$
$m_{muối} = 0,02.152 = 3,04(gam)$
c)
$n_{M_{FeSO_4}} = \dfrac{0,02}{0,2} = 0,1M$