Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Định hướng tư duy giải
Nhận thấy
82 , 38 855 = 1373 14250
=> rất lẻ
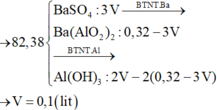

Đáp án C


● Nhận xét: Khi gặp dạng bài này ta nên xét trường hợp dễ xảy ra nhất, đó là Al(OH)3 bị tan một phần.

Đáp án B
+ n A l 2 ( S O 4 ) 3 = 0 , 05 m o l ; n B a ( O H ) 2 = 0 , 15 ; n K O H = 0 , 3 x . + n B a S O 4 = n B a 2 + = n S O 4 2 - = 0 , 15 n A l ( O H ) 3 = 36 , 9 - 0 , 15 . 233 78 = 0 , 025 < n A l 3 + = 0 , 1 + K + : 0 , 3 x A l O 2 - : 0 , 1 - 0 , 025 = 0 , 075 ⏟ d d s a u p h ả n ứ n g ⇒ 0 , 3 x = 0 , 075 ⇒ x = 0 , 25

Chọn D.
nBa(OH)2 đầu = 0.15 => nOH- = 0.3
nAl2(SO4)3 = 0.25x => nAl3+ = 0.5x và nSO4(2-) = 0.75x
Khi cho 150ml Ba(OH)2 vào dd thu được 42.75g kết tủa
Thêm tiếp 200ml
=> m kết tủa theo lí thuyết = 350*42.75/150 = 99.75g > 94.2375g
=> Lúc đầu chưa tạo kết tủa cực đại, Al2(SO4)3 dư ; sau khi thêm Ba(OH)2 vào thì pứ tạo kết tủa
lớn nhất và sau đó Ba(OH)2 dư sẽ hòa tan thêm một phần kết tủa
+ Khi chưa thêm: (tính theo nBa(OH)2)
Ba2+ + SO42- ---> BaSO4
0.15 0.15 0.15
Al3+ + 3OH- ----> Al(OH)3
0.1 0.3 0.1
+ Khi thêm Ba(OH)2 vào: (tính theo nAl2(SO4)3)
Ba2+ + SO42- ---> BaSO4
0.75x-0.15 0.75x-0.15
Al3+ + 3OH- ---> Al(OH)3
0.5x-0.1 1.5x-0.3 0.5x-0.1
OH- dư + Al(OH)3 --->AlO2- + 2 H2O
0.4-1.5x+0.3 0.7-1.5x
Ta có:
m kết tủa lúc sau = m kết tủa ban đầu + mBaSO4 sau + mAl(OH)3 chưa tan lúc sau = 42.75 + 233*(0.75x-0.15) +
78*(0.5x-0.1-0.7+1.5x)
=> 330.75x - 54.6 = 94.2375
=> x = 0.45

Chọn đáp án C
Chú ý :
(1). Trong bài toán này người ta không vớt kết tủa lần đầu ra mà cứ để yên rồi đổ thêm Ba(OH)2 vào.
(2). Để mò ra đáp án nhanh bài toán này các bạn cần tư duy nhanh xem lượng kết tủa ở lần 1 và 2 có bị tan phần nào không.Điều này khá đơn giản.
+Nhìn nhanh qua đáp án cũng khẳng định được ở lần 1 muối sunfat có dư.
+Khi đổ thêm Ba(OH)2 dễ thấy Al(OH)3 bị tan vì khi x = 0,45 vẫn bị tan
Khi đó ta có
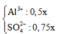
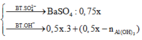
![]()
![]()
Vậy
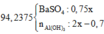
![]()
![]()
Bài này các bạn cũng có thể dùng thủ đoạn truyền thống “thử đáp án”
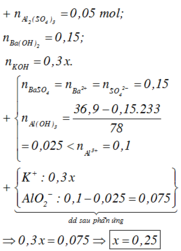
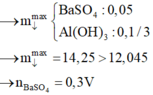
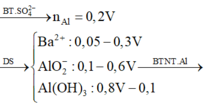
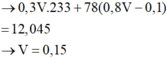

Định hướng tư duy giải
Nhận thấy
9 , 636 855 = 1088 7125
=> rất lẻ