Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nMg = \(\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + H2SO4 ---> MgSO4 + H2
Theo PT: \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\)
=> \(V_{H_2}=0,2.22,4=4,48\left(lít\right)\)
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)

a)
$Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe +3 CO_2$
$Fe + 2HCl \to FeCl_2 + H_2$
$RO + H_2 \xrightarrow{t^o} R + H_2O$
b)
Coi m = 160(gam)$
Suy ra: $n_{Fe_2O_3} = 1(mol)$
Theo PTHH :
$n_{RO} = n_{H_2} = n_{Fe} = 2n_{Fe_2O_3} = 2(mol)$
$M_{RO} = R + 16 = \dfrac{160}{2} = 80 \Rightarrow R = 64(Cu)$
Vậy oxit là CuO

Vì đồng không tác dụng với HCl loãng :
1) Chất rắn không tan là đồng nên :
\(m_{Al}=11,8-6,4=5,4\left(g\right)\)
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Pt : \(2Al+6HCl\rightarrow2AlCl_3+3H_2|\)
2 6 2 3
0,2 0,3
\(n_{H2}=\dfrac{0,2.3}{2}=0,3\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
2) Có : \(m_{Cu}=6,4\left(g\right)\)
\(n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
Pt : \(2Al+6H_2SO_{4đặc}\underrightarrow{t^o}Al_2\left(SO_4\right)_3+3SO_2+6H_2O|\)
2 6 1 3 6
0,2 0,3
\(Cu+2H_2SO_{4đặc}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O|\)
1 2 1 1 2
0,1 0,1
\(n_{SO2\left(tổng\right)}=0,3+0,1=0,4\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,4.22,4=8,96\left(l\right)\)
Chúc bạn học tốt

a) Zn + 2HCl → ZnCl2 + H2
nZn = 9,75 : 65 = 0,15 mol
Theo ptpư
nH2 = nZn = 0,15 mol
VH2 = 0,15 . 22,4 = 3,36 lit
b) CuO + H2 →H2O + Cu
nCuO = 20 : 80 = 0,25 mol
nCuO p/ư = nH2 = 0,15 mol
=> Dư CuO
nCu thu được= nH2 = 0,15 mol
mCu= 0,15 x 64 = 9,6 gam

a) nAl=2,7/27=0,1(mol)
nHCl=14,6/36,5= 0,4(mol)
PTHH: 2Al +6 HCl -> 2 AlCl3 +3 H2
Ta có: 0,1/2 < 0,6/4
=> HCl dư, Al hết, tính theo nAl
=> nAlCl3=nAl=0,1(mol)
=> mAlCl3=0,1.133,5=13,35(g)
b) nH2= 3/2. nAl=3/2. 0,1=0,15(mol)
=>V(H2,đktc)=0,15.22,4=3,36(l)
c) mFe2O3(nguyên chất)= 80%. 38,4=30,72(g)
=>nFe2O3= 30,72/160=0,192(mol)
PTHH: Fe2O3 + 3 H2 -to->2 Fe +3 H2O
Ta có: 0,192/1 > 0,15/3
=> H2 hết, Fe2O3 dư, tính theo nH2
=> nFe= 2/3. nH2= 2/3. 0,15=0,1(mol)
=>mFe=0,1.56=5,6(g)
a,\(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right);n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl → 2AlCl3 + 3H2
Mol: 0,1 0,1 0,15
Tỉ lệ:\(\dfrac{0,1}{2}< \dfrac{0,4}{6}\) ⇒ Al pứ hết,HCl dư
\(\Rightarrow m_{AlCl_3}=0,1.133,5=13,35\left(g\right)\)
b,\(V_{H_2}=0,15.22,4=3,36\left(l\right)\)
c,\(m_{Fe_2O_3\left(tinhkhiét\right)}=38,4.\left(100\%-20\%\right)=30,72\left(g\right)\)
⇒\(n_{Fe_2O_3}=\dfrac{30,72}{160}=0,192\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol : 0,15 0,1
Tỉ lệ:\(\dfrac{0,192}{1}>\dfrac{0,15}{3}\)⇒ Fe2O3 dư,H2 hết
=> mFe = 0,1.56 =5,6 (g)

\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 0,25.........0,5.........0,25.......0,25\left(mol\right)\\ a.V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b.m_{HCl}=0,5.36,5=18,25\left(g\right)\\ c.n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\\ Fe_2O_3+3H_2\underrightarrow{^{to}}2Fe+3H_2O\\ Vì:\dfrac{0,25}{3}< \dfrac{0,1}{1}\\ \Rightarrow Fe_2O_3dư\\ n_{Fe}=\dfrac{2}{3}.0,25=\dfrac{1}{6}\left(mol\right)\\ \Rightarrow m_{Fe}=\dfrac{1}{6}.56\approx9,333\left(g\right)\)
a,\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,25 0,5 0,25
\(\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)
b,\(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
c,\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol: 0,25 \(\dfrac{1}{6}\)
Ta có: \(\dfrac{0,1}{1}>\dfrac{0,25}{3}\)⇒ Fe2O3 dư, H2 hết
\(m_{Fe}=\dfrac{1}{6}.56=9,33\left(g\right)\)

\(a,n_{\left(CH_3COO\right)_2Mg}=\dfrac{7,1}{142}=0,05\left(mol\right)\)
PTHH: \(Mg+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+H_2\uparrow\)
0,1<----------------0,05-------------->0,05
\(\rightarrow V_{H_2}=0,05.22,4=1,12\left(l\right)\\ b,C\%_{CH_3COOH}=\dfrac{0,1.60}{100}.100\%=6\%\)
\(c,n_{C_2H_5OH}=\dfrac{6,9}{46}=0,15\left(mol\right)\)
PTHH: \(CH_3COOH+C_2H_5OH\xrightarrow[H_2SO_{4\left(đặc\right)}]{t^o}CH_3COOC_2H_5+H_2O\)
bđ 0,1 0,15
pư 0,1 0,1
spư 0 0,05 0,1
\(\rightarrow m_{este}=0,1.80\%.88=7,04\left(g\right)\)
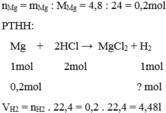
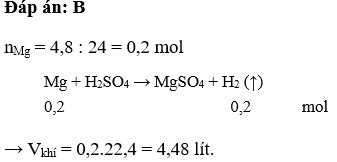
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{H_2}=n_{Mg}=0,2\left(mol\right)\\ n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\\ CuO+H_2\underrightarrow{^{to}}Cu+H_2O\\ Vì:\dfrac{0,25}{1}>\dfrac{0,2}{1}\\ \Rightarrow CuOdư\\ \Rightarrow n_{Cu}=n_{H_2}=0,2\left(mol\right)\\ m_{Cu}=0,2.64=12,8\left(g\right)\)
\(n_{Mg}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,2 0,2
\(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
Pt : \(H_2+CuO\rightarrow\left(t_o\right)Cu+H_2O|\)
1 1 1 1
0,2 0,25 0,2
Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{0,25}{1}\)
⇒ H2 phản ứng hết , CuO dư
⇒ Tính toán dựa vào số mol của H2
\(n_{Cu}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{Cu}=0,2.64=12,8\left(g\right)\)
Chúc bạn học tốt