Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

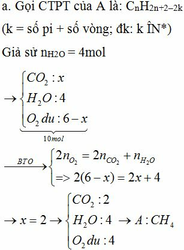
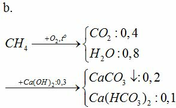
pt:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,3 → 0,3 0,3
CO2 + CaCO3 + H2O → Ca(HCO3)2
0,1 → 0,1 0,1
m dd tăng = mCO2 + mH2O – mCaCO3 = 12g

Ở cùng điều kiện nhiệt độ và áp suất thì tỉ lệ về thể tích cũng chính là tỉ lệ về số mol

⇒ Chọn B.

Có phương trình cháy
4NH3+3O2->2N2+6H2O
CxHy+(x+y/4)O2->xCO2+(y/2)H2O
Theo dữ kiện bài toán sau khi đốt cháy tạo 100 ml ni tơ
Thực tết thhu được thể tích N2 nhỏ hơn 2 lần hỗn hợp đầu
->V NH3 ban đầu là 100*2=200ml
->V CxHy ban đầu = 100ml
Sau khi đốt tạo 550-250=300 ml CO2
và 1250-550-300=400 ml nước
Có tỉ lệ
CxHy+(x+y/4)O2->xCO2+(y/2)H2O
100------------------300--------400
->x=3
y=8
Vậy CT C3H8

a)

CxH2x +2 + (3x+1)/2O2 → t ∘ x CO2 + (x+1) H2O
CyH2y + 3y/2O2 → t ∘ y CO2 + y H2O
CzH2z-2 + (3z-1)/2O2 → t ∘ zCO2 + (z-1) H2O
Khi đốt cháy hỗn hợp A thu được CO2 và H2O. Cho sản phẩm qua Ca(OH)2 dư thì khối lượng bình tăng chính là khối lượng của H2O và CO2
=> mCO2 + mH2O = 9,56 (g)
CO2 + Ca(OH)2 → CaCO3↓ + H2O
nCO2 = nCaCO3 = 16/100 = 0,16 (mol)
=> nH2O = (9,56 – 0,16.44)/18 = 0,14 (mol)
Ta có hệ phương trình:
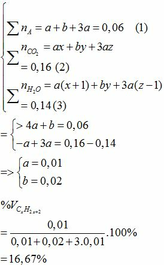
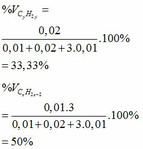
b)
thế a, b vào (2) => 0,01x + 0,02y + 3.0,01z = 0,16
=> x + y +3z = 16
Vì có 2 hidrocacbon bằng nhau và bằng một nửa số cacbon của hidrocacbon còn lại nên có các trường hợp sau:
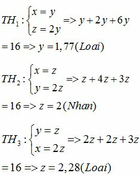
Vậy công thức phân tử của 3 hidrocacbon là: C2H6; C2H4 và C2H2

Y gồm \(\left\{{}\begin{matrix}A:a\left(mol\right)\\CO_2:b\left(mol\right)\\H_2O:c\left(mol\right)\end{matrix}\right.\)
Z gồm \(\left\{{}\begin{matrix}A:a\left(mol\right)\\CO_2:b\left(mol\right)\end{matrix}\right.\)
Do nZ = 50%.nY
=> a + b = 0,5a + 0,5b + 0,5c
=> \(c=a+b\)
Khí thoát ra khỏi dd NaOH là khí A
\(n_{CO_2}=83,33\%.n_Z\)
=> b = 0,8333.(a + b)
=> 5a = b
=> Y gồm \(\left\{{}\begin{matrix}A:a\left(mol\right)\\CO_2:5a\left(mol\right)\\H_2O:6a\left(mol\right)\end{matrix}\right.\)
=> nC(A pư) : nH(A pư) = 5a : 12a = 5 : 12
=> CTPT: (C5H12)n
Chọn n = 1 thỏa mãn => CTPT: C5H12

Khi cho hỗn hợp A qua dung dịch brom dư, có phản ứng :
C 2 H 2 + 2 Br 2 → C 2 H 2 Br 4
Vì phản ứng xảy ra hoàn toàn và có hai khí thoát ra khỏi dung dịch brom, nên hai khí đó là CH 4 và C n H 2 n + 2
Theo đề bài V C 2 H 2 tham gia phản ứng là : 0,896 - 0,448 = 0,448 (lít).
Vậy số mol C 2 H 2 là 0,448/22,4 = 0,02 mol
Gọi số mol của CH 4 là X. Theo bài => số mol của C n H 2 n + 2 cũng là x.
Vậy ta có : x + x = 0,448/22,4 = 0,02 => x = 0,01
Phương trình hoá học của phản ứng đốt cháy hỗn hợp :
2 C 2 H 2 + 5 O 2 → 4 CO 2 + 2 H 2 O
CH 4 + 2 O 2 → CO 2 + 2 H 2 O
2 C n H 2 n + 2 + (3n+1) O 2 → 2n CO 2 + 2(n+1) H 2 O
Vậy ta có : n CO 2 = 0,04 + 0,01 + 0,01n = 3,08/44 => n = 2
Công thức phân tử của hiđrocacbon X là C 2 H 6
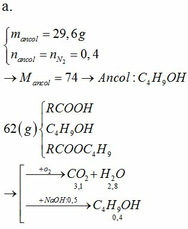
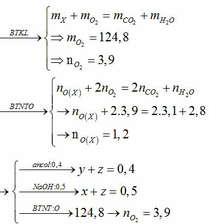
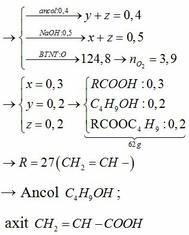
làm sao biết được đó là ankan và Nito có phản ứng với O2 ra NO mà ?
Giả sử các khí đều đo ở đktc
\(CTHH:C_nH_{2n+2}\)(n là số tự nhiên khác 0)
\(V_{H_2O}=1,4-0,8=0,6\left(l\right)\)
\(V_{CO_2}=0,8-0,4=0,4\left(mol\right)\)
=> \(\left\{{}\begin{matrix}n_{H_2O}=\frac{0,6}{22,4}=\frac{3}{112}\left(mol\right)\\n_{CO_2}=\frac{0,4}{22,4}=\frac{1}{56}\left(mol\right)\end{matrix}\right.\)
Bảo toàn H: \(n_{H\left(X\right)}=2.n_{H_2O}=\frac{3}{56}\left(mol\right)\)
Bảo toàn C: \(n_{C\left(X\right)}=n_{CO_2}=\frac{1}{56}\left(mol\right)\)
=> \(\frac{n_C}{n_H}=\frac{\frac{1}{56}}{\frac{3}{56}}=\frac{1}{3}\) => \(\frac{n}{2n+2}=\frac{1}{3}=>n=2\)
=> CTHH: \(C_2H_6\)