
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

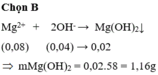

nNaHCO3 = 0,03; nK2CO3 = 0,06
nHCI = 0,02 và nNaHSO4 = 0,06 —> nH+ = 0,08
nHCO3- : nCO32- = 1 : 2 —> Đặt x, 2x là số
mol HCO3- và CO32- phản ứng.
—> nH+ = x + 2.2x = 0,08 => x = 0,016
—> nCO2 = x + 2x = 0,048
—>V=1,0752 lít
Dung dịch X chứa HCO3- dư (0,03 - x = 0,014), CO32- dư (0,06 - 2x = 0,028),
SO42-(0,06) và các ion khác.
nKOH = 0,06 —> Quá đủ để chuyển HCO3- thành CO32-.
nBaCl2 = 0,15 —> BaCO3 (0,014 + 0,028 =0,042) và BaSO4 (0,06)
→ m ↓ = 22 , 254
Đáp án A

Chọn A
Fe2+ + 2OH- → Fe(OH)2↓
(0,04) (0,02) → 0,01
mFe(OH)2 = 0,01.90 = 0,9g

Đáp án C
n H + =0,02 + 0,06 = 0,08 mol
n H C O 3 - = 0,03 mol
n C O 3 2 - =0,06 mol
Đổ từ từ dung dịch axit vào hỗn hợp muối
CO32- + H+ → HCO3-
0,06 0,06 0,06
HCO3- + H+ →CO2 + H2O
0,02 0,02 mol
=> V = 0,448 l
HCO3- + OH- → CO32- + H2O
0,06 0,06 mol
n S O 4 2 - = 0 , 06 m o l
n B a 2 + = 0,15 mol
⇒ n B a S O 4 = n B a C O 3 = 0,06 mol
=>Vậy m = 0,06.233 + 0,06.197 = 25,8 gam

Đáp án : C
0 , 03 m o l N a H C O 3 0 , 06 m o l K 2 C O 3 nhỏ từ từ 0 , 02 m o l H C l 0 , 06 m o l K H S O 4
=> 2 muối kiềm sẽ phản ứng theo tỉ lệ mol 1:2
Đặt số mol NaHCO3 phản ứng là x => số mol KCO3 phản ứng là 2x
=> nH+ = 0,02 + 0,06 = x + 2.2x => x = 0,016 mol
=> Sau phản ứng có : 0,014 mol HCO3- ; 0,028 mol CO32- và 0,06 mo SO42-
Khi cho X vào dung dịch chứa : 0,06 mol KOH và 0,15 mol BaCl2
=> nCO3 = 0,014 + 0,028 = 0,042 mol ; nSO4 = 0,06 mol
=> m kết tủa = mBaCO3 + mBaSO4 = 22,254g

Đáp án B
Cho từ từ 0,03 mol NaHCO3 và 0,06 mol K2CO3 vào 0,02 mol HCl và 0,06 mol NaHSO4 thu được dung dịch X
