Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. \(n_{Zn}=\dfrac{2,6}{65}=0,04\left(mol\right)\)
\(PTHH:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
- Mol theo PTHH : \(1:1:1:1\)
- Mol theo phản ứng : \(0,04\rightarrow0,04\rightarrow0,04\rightarrow0,04\)
\(\Rightarrow m_{ZnSO_4}=n_{ZnSO_4}.M_{ZnSO_4}=0,04.161=6,44\left(g\right)\)
b. Từ a. suy ra : \(V_{H_2}=n_{H_2}.22,4=0,04.22,4=0,896\left(l\right)\)
c. Từ a. suy ra : \(n_{H_2}=0,04\left(mol\right)\)
\(PTHH:H_2+PbO\underrightarrow{t^o}Pb+H_2O\)
- Mol theo PTHH : \(1:1:1:1\)
- Mol theo phản ứng : \(0,04\rightarrow0,04\rightarrow0,04\rightarrow0,04\)
\(\Rightarrow m_{Pb}=n_{Pb}.M_{Pb}=0,04.207=8,28\left(g\right)\)

a) nAl = 43,2/27 = 1,6 mol
2Al + 6HCl → 2AlCl3 + 3H2
1,6 \(\dfrac{1,6\times3}{2}=2,4\)
→ nH2 = 2,4 mol → VH2 = 2,4 x 22, 4 = 53,76 lít
b) nCuO = 64/80 = 0,8 mol
nH2 = 2,4 mol
→ H2 dư, phương trình tính theo số mol của CuO
CuO + H2 → Cu + H2O
0,8 0,8 0,8 0,8
Chất rắn sau phản ứng có Cu
mCu = 0,8 x 64 = 51,2 gam

\(n_{HCl}=0.2\cdot1=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(........0.2..............0.1\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(n_{CuO}=\dfrac{16}{80}=0.2\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{t^0}}Cu+H_2O\)
\(0.1.......0.1....0.1\)
\(\Rightarrow CuOdư\)
\(m_{Cu}=0.1\cdot64=6.4\left(g\right)\)

Ta có: \(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
\(PTHH:\)
\(Fe+2HCl--->FeCl_2+H_2\left(1\right)\)
\(CuO+H_2\overset{t^o}{--->}Cu+H_2O\left(2\right)\)
a. Theo PT(1): \(n_{H_2}=n_{Fe}=0,15\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,15.22,4=3,36\left(lít\right)\)
b. Ta thấy: \(\dfrac{0,15}{1}< \dfrac{0,2}{1}\)
Vậy CuO dư.
Theo PT(2): \(n_{Cu}=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)\)

Zn+2HCl->Zncl2+H2
0,4----0,8----0,4----0,4
n Zn=0,4 mol
VH2=0,4.22,4=8,96l
m ZnCl2=0,4.136=54,4g
2H2+O2-to>2H2O
0,4------0,2----0,4
n O2=0,2 mol
=>pứ hết
=>m H2O=0,4.18=7,2g
a.b.\(n_{Zn}=\dfrac{26}{65}=0,4mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,4 0,4 0,4 ( mol )
\(m_{ZnCl_2}=0,4.136=54,4g\)
\(V_{H_2}=0,4.22,4=8,96l\)
c.\(n_{O_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
0,4 = 0,2 ( mol )
0,4 0,2 0,4 ( mol )
\(m_{H_2O}=0,4.18=7,2g\)
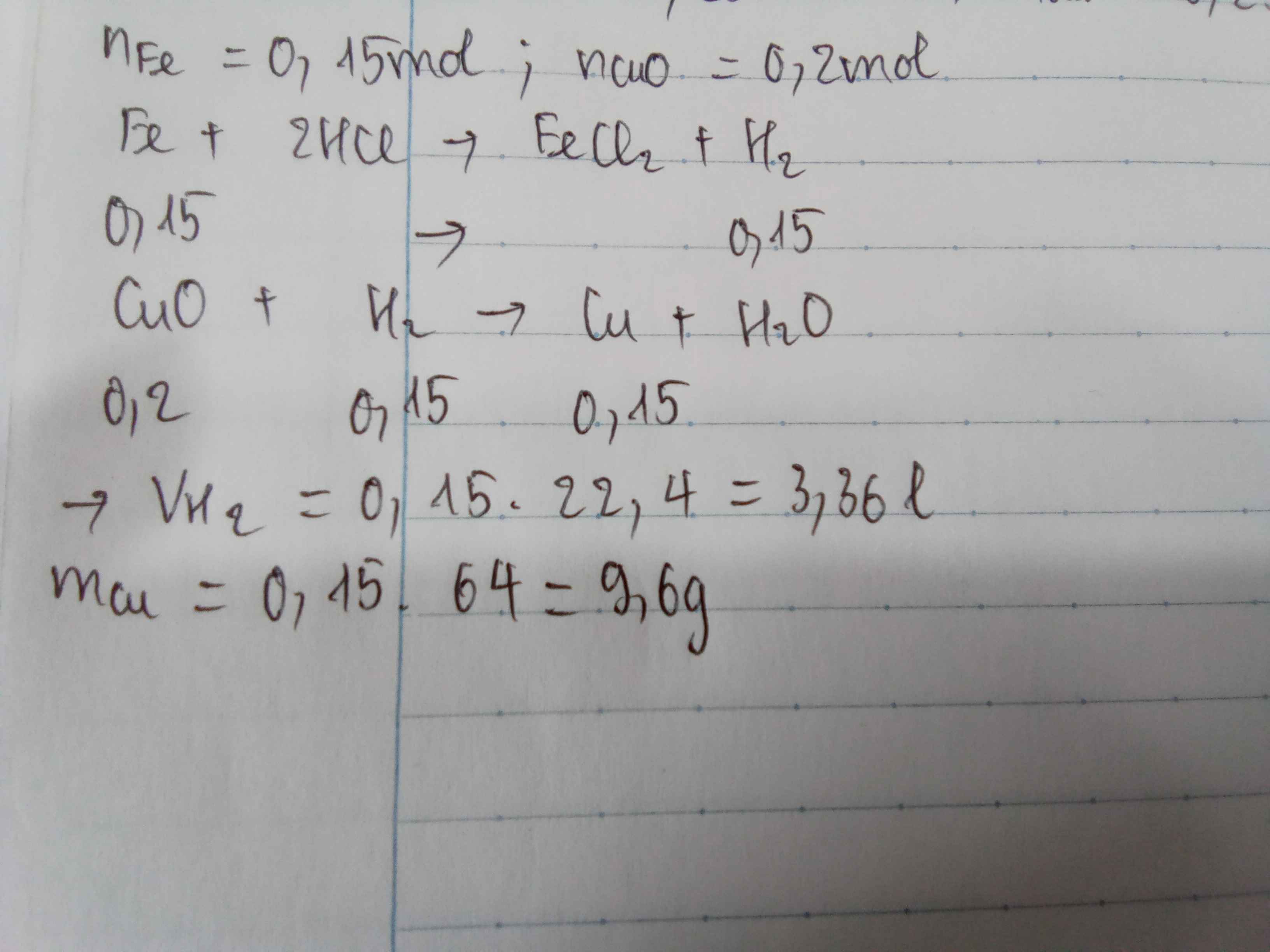

n\(_{Zn}\)= \(\dfrac{3,25}{65}\)= 0,05 (mol)
PTHH:Zn + 2HCl ----> ZnCl2 + H2\(\uparrow\)
mol: 0,05-->0,1------------------>0,05
PTHH:PbO + H2 --to--> Pb + H2O
mol:_0,05<-0,05
m = 0,05 . 207 = 10,35 (g)
nZn = \(\dfrac{3,25}{65}\) = 0,05 mol
Zn + 2HCl -> ZnCl2 + H2
0,05 ->0,05
VH2 = 0,05 . 22,4 = 1,12 (l)
H2 + PbO -> Pb + H2
0,05-> 0,05
m = 0,05 .223 = 11,15 g