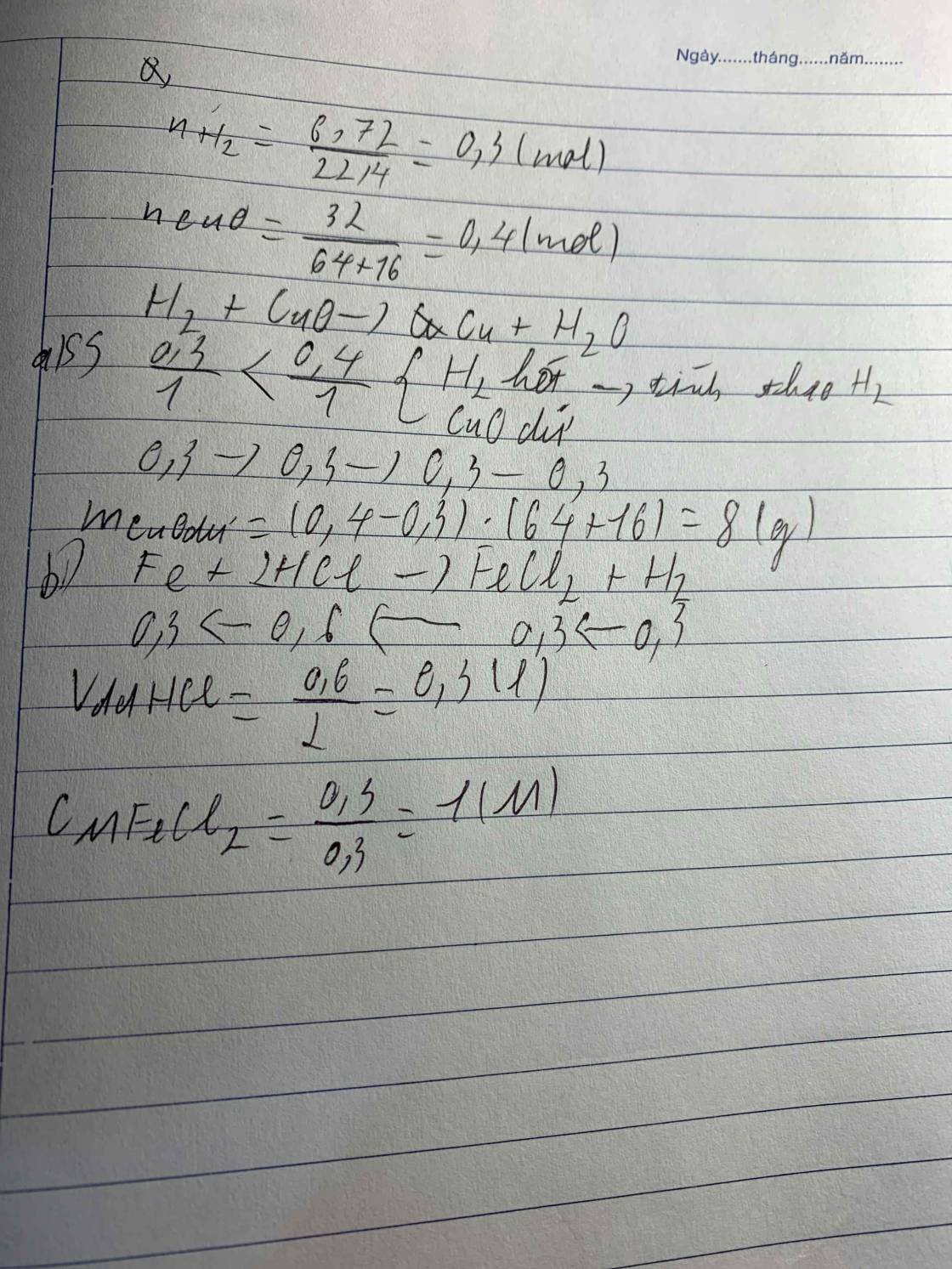Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2---------------------->0,3
=> VH2 = 0,3.22,4 = 6,72 (l)
b)
\(n_{CuO}=\dfrac{32}{80}=0,4\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,3}{1}\) => CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
0,3<--0,3------->0,3
=> Rắn sau pư gồm \(\left\{{}\begin{matrix}Cu:0,3\left(mol\right)\\CuO\left(dư\right):0,1\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,3.64}{0,3.64+0,1.80}.100\%=70,59\%\\\%m_{CuO}=\dfrac{0,1.80}{0,3.64+0,1.80}.100\%=29,41\%\end{matrix}\right.\)

a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b, \(n_{Fe_2O_3}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,3}{3}\), ta được Fe2O3 dư.
Theo PT: \(n_{Fe_2O_3\left(pư\right)}=\dfrac{1}{3}n_{H_2}=0,1\left(mol\right)\Rightarrow n_{Fe_2O_3\left(dư\right)}=0,3-0,1=0,2\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,2.160=32\left(g\right)\)

\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
a)\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,6 0,3
\(C_M=\dfrac{0,6}{0,4}=1,5M\)
b)\(n_{CuO}=\dfrac{32}{80}=0,4mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,4 0,3 0,3
Sau phản ứng CuO dư và dư \(\left(0,4-0,3\right)\cdot80=8g\)
\(m_{rắn}=m_{Cu}=0,3\cdot64=19,2g\)

a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{Fe_2O_3}=\dfrac{6,4}{160}=0,04\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,04}{1}< \dfrac{0,2}{3}\), ta được H2 dư.
Theo PT: \(n_{H_2\left(pư\right)}=3n_{Fe_2O_3}=0,12\left(mol\right)\Rightarrow n_{H_2\left(dư\right)}=0,2-0,12=0,08\left(mol\right)\)
\(\Rightarrow m_{H_2\left(dư\right)}=0,08.2=0,16\left(g\right)\)
Theo PT: \(n_{Fe}=2n_{Fe_2O_3}=0,08\left(mol\right)\Rightarrow m_{Fe}=0,08.56=4,48\left(g\right)\)

a.b.c.\(n_{Al}=\dfrac{2,7}{27}=0,1mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1 0,1 0,15 ( mol )
\(V_{H_2}=0,15.22,4=3,36l\)
\(m_{AlCl_3}=0,1.133,5=13,35g\)
d.\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,15 0,1 ( mol )
\(m_{Fe}=0,1.56=5,6g\)

\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(m\right)\);\(n_{Fe_2O_3}=\dfrac{80}{160}=0,5\left(m\right)\)
\(PTHH:Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\)
ta có tỉ lệ:\(\dfrac{0,5}{1}>\dfrac{0,5}{3}\)=>\(Fe_2O_3\) dư
H2 phản ứng hết
\(PTHH:Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\)
tỉ lệ :1 3 2 3
số mol :0,17 0,5 0,3 0,5
\(m_{Fe_2O_3}=0,3.160=48\left(g\right)\)

a) \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{0,4}{6}\) => Al hết, HCl dư
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,1--->0,3------>0,1---->0,15
=> mHCl = (0,4 - 0,3).36,5 = 3,65 (g)
b) VH2 = 0,15.22,4 = 3,36 (l)
\(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{2,7}{27}=0,1mol\)
\(n_{HCl}=\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{14,6}{36,5}=0,4mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1 < 0,4 ( mol )
0,1 0,3 0,15 ( mol )
a. Chất còn dư là HCl
\(m_{HCl}=n_{HCl}.M_{HCl}=\left(0,4-0,3\right).36,5=3,65g\)
\(V_{H_2}=n_{H_2}.22,4=0,15.22,4=3,36l\)