Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt a,b là số mol Mg, R trong 8 gam A. Đặt x,y là hoá trị thấp cao của R
mA = 24a + bR = 8 (1)
Với HCl -> 2a + bx = 0,2 .2 (2)
Trong 9,6 gam A ( gấp 1,2 lần 8 gam A ) chứa 1,2a và 1,2b mol Mg, R
Với Cl2 -> 2 . 1,2a + 1,2by = 2 ( 30,9 - 9,6 ) / 71 (3)
Với 1 ≤ x ≤ y ≤ 3 -> Chọn x = 2; y = 3
(2)(3) -> a = b = 0,1
(1) -> R= 56 -> = Fe

2Fe + 3 Cl 2 → t ° 2Fe Cl 3 ( M FeCl 3 = 162,5 gam)
Cu + Cl 2 → t ° Cu Cl 2
Fe + 2HCl → Fe Cl 2 + H 2 ( M FeCl 2 = 127 gam)
n Fe = x mol
Theo đề bài và phương trình hóa học trên ta có:
127x = 25,4 => 0,2 mol
162,5x + 135y = 59,5. Thay x = 0,2 vào phương trình, ta có:
32,5 + 135y = 59,5 => y = 0,2
m FeCl 3 = 0,2 x 162,5 = 32,5g
m CuCl 2 = 0,2 x 135 = 27g
% m FeCl 3 = 32,5 : (32,5 + 27).100% = 54,62%
% m CuCl 2 = 100% - 54,62% = 45,38%

1.
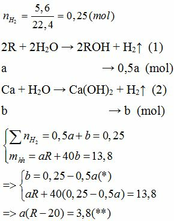
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
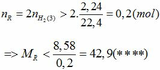
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
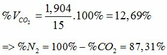
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
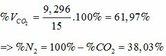

m axit cần dùng = 0,2 x 2 x 36,5 = 14,6g
m dung dịch HCl = 146g => V dd HCl = 146/1 = 146ml

a, Đặt kim loại trung bình là R \(\rightarrow \) R hóa trị II
\(PTHH:R+2HCl\to RCl_2+H_2\\ \Rightarrow n_R=n_{H_2}=\dfrac{4,48}{22,4}=0,2(mol)\\ \Rightarrow M_R=\dfrac{6,5}{0,2}=32,5(g/mol)\)
Vậy 2 KL đó là Mg (24) và Ca (40)
\(b,\) Đặt \((n_{Mg};n_{Ca})=(x;y)(mol)\)
\(\Rightarrow \begin{cases} 24x+40y=6,5\\ x+y=n_{H_2}=0,2 \end{cases}\Rightarrow \begin{cases} x=0,09375(mol)\\ y=0,10625(mol) \end{cases}\\ \Rightarrow \begin{cases} m_{Mg}=2,25(g)\\ m_{Ca}=4,25(g) \end{cases}\)

Gọi CT oxit là M2Om
Mol H2 TN1=0,06 mol
Mol H2 TN2=0,045 mol
M2Om + mH2→ 2M + mH2O
0,06/m mol<=0,06 mol. =>0,12/m mol
=>0,06(2M+16m)/m=3,48
2M + 2nHCl→ 2MCln + nH2
0,12/m mol. 0,045 mol
⇒⇒0,045.2/n=0,12/m⇒⇒m=8/3; n=2 tm
Thay m=8/3 vào công thức tính m có M=56 FeFe
Oxit là Fe3O4 vì n=8/3

Kl Oxi: m(O) = [m(0xit) - m(Kim loai)] = (22,3 - 14,3) = 8
====> n(0) = 8/16 = 0,5(m0l)
Theo bảo toàn nguyên tố ta có:
+, n(H20) = n(0) = 0,5 (mol)
+, n(HCl) = 2n(H20) = 0,5*2 = 1 (m0l)
Theo bảo toàn khối lượng:
m(Oxit) + m(Axit) = m(Muối) + m(Nước)
=====> m(Muối) = m(0xit) + m(Axit) - m(H20) = 22,3 + 36,5*1 - 18*0,5 = 49,8

Hỗn hợp khí B gồm CO và CO2 khi tác dụng với dd chứa 0,025 mol Ca(OH)2 chắc chắc tạo 2 muối
Ta có: \(n_{CaCO_3}=\dfrac{2}{100}=0,02\left(mol\right)\)
PTHH: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
0,02______0,02______0,02 (mol)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
0,01_____0,005_______0,005 (mol)
\(\Rightarrow n_{CO_2}=0,03\left(mol\right)\) \(\Rightarrow m_{CO_2}=0,03\cdot44=1,32\left(g\right)\)
Bảo toàn nguyên tố: \(n_{CO\left(p/ứ\right)}=n_{CO_2}=0,03\left(mol\right)\) \(\Rightarrow m_{CO}=0,03\cdot28=0,84\left(g\right)\)
Bảo toàn khối lượng: \(m_A=m_{oxit}+m_{CO}-m_{CO_2}=1,12\left(g\right)\)
PTHH: \(2A+2zHCl\rightarrow ACl_z+zH_2\uparrow\) (z là hóa trị của A)
Ta có: \(n_{H_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
\(\Rightarrow n_A=\dfrac{0,04}{z}\left(mol\right)\) \(\Rightarrow M_A=\dfrac{1,12}{\dfrac{0,04}{z}}=28z\)
Ta thấy với \(z=2\) thì \(M_A=56\) \(\Rightarrow\) Kim loại A là Fe
Gọi công thức oxit cần tìm là FexOy
Bảo toàn Oxi: \(n_{O\left(oxit\right)}=2n_{CO_2}-n_{CO}=0,03\left(mol\right)\)
Xét tỉ lệ \(x:y=0,02:0,03=2:3\)
Vậy công thức oxit là Fe2O3
Giả sử 24,8 gam hỗn hợp toàn là kim loại, không có oxit.
--> m Cl = 55,5 - 24,8 = 30,7 gam.
Cứ 1 mol R sau khi thành RCl2 thì khối lượng tăng lên 71 gam.
--> n R = 30,7/71 = 0,4323943 mol
--> MR = 24,8/0,4323943 = 57,355057 (1).
Giả sử 24,8 gam hỗn hợp toàn là oxit của R, không có kim loại.
Cứ 1 mol RO sau khi thành RCl2 thì khối lượng tăng lên 55 gam.
--> n RO = 30,7/55 = 0,5581818 mol
--> M RO = 24,8/0,5581818 = 44,429968
--> MR = 44,429968 - 16 = 28,429968 (2).
Từ (1) và (2) --> 28,429968 < MR < 57,355057.
--> Chọn MR = 40 với R là Ca.
Gọi R là kim kiềm thổ ( Hóa trị II ) chưa biết
Gọi x ; y là số mol của R và RO
R + 2HCl --> RCl2 + H2
x ----------------> x
RO + 2HCl --> RCl2 + H2O
y -------------------> y
n RCl2 = 55,5 / (MR + 71)
Ta lại có
x.MR + y.(MR + 16) = 24,8
Ta có hệ pt sau :
{ x + y = 55,5 / (MR + 71)
{ x.MR + y.(MR + 16) = 24,8
Ta có :
D = (MR + 16) - MR = 16
Dx = 55,5(MR + 16) / (MR + 71) - 24,8
= [ 55,5(MR + 16) - 24,8(MR + 71)] / (MR + 71)
= ( 30,7MR - 872,8 ) / (MR + 71 )
Dy = 24,8 - MR.55,5 / (MR + 71)
= [ 24,8.(MR + 71) - MR.55,5 ] / (MR + 71)
= ( -30,7MR + 1760,8 ) / (MR + 71)
Chỉ có 1 TH là hệ pt có 1 ẩn
=> x = Dx/D = 16.( 30,7MR - 872,8 ) / (MR + 71 ) = ( 491,2MR - 13964,8 ) / (MR + 71 )
=> y = Dy/D = 16.( -30,7MR + 1760,8 ) / (MR + 71) = ( -491,2MR + 28172,8) / (MR + 71 )
Vì x ; y là số mol ; MR là khối lượng của kim loại kiềm thổ nên x ; y ; MR > 0
. MR + 71 > 0
<=> MR > -71 (1)
Thì 491,2MR - 13964,8 > 0
<=> MR > 8728/307 (2)
Và -491,2MR + 28172,8 > 0
<=> MR < 17608/307 (3)
Từ (1) ; (2) ;(3) => 8728/307 < MR < 17608/307
Từ đó chỉ có 1 chất là Canxi ( Ca)