Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cho 4,72 gam hỗn hợp bột gồm các chất Fe, FeO và Fe2O3 tác dụng với CO ở nhiệt độ cao. Phản ứng xong thu được 3,92 gam Fe. Nếu ngâm cùng lượng hỗn hợp các chất trên trong dung dịch CuSO4 dư, phản ứng xong khối lượng chất rắn thu được là 4,96 gam. Khối lượng (gam) Fe, Fe2O3 và FeO trong hỗn hợp ban đầu lần lượt là
A. 1,68; 1,44; 1,6
B. 1,6; 1,54; 1,64

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH :
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,15 0,3 0,15 0,15
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
0,1 0,6 0,2 0,3
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
\(m_{Fe_2O_3}=15-8,4=6,6\left(g\right)\)
\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
\(C_{M\left(HCl\right)}=\dfrac{0,3+0,6}{0,05}=18\left(M\right)\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
0,35 0,35
\(m_{Fe\left(OH\right)_2}=0,35.90=31,5\left(g\right)\)

2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
x…………3/2.x
F e + C u S O 4 → F e S O 4 + C u
y……..y
Al phản ứng hết với C u S O 4 sau đó Fe mới phản ứng với C u S O 4 . Vì sau phản ứng thu được rắn Y gồm 2 kim loại nên Al đã tan hết và Fe có thể đã phản ứng 1 phần hoặc chưa phản ứng. 2 kim loại trong Y là Fe và Cu.
⇒ n C u = n C u S O 4 = 0,2.1 = 0,2 mol
⇒ m F e dư = m Y - m C u = 15,68 - 0,2.64 = 2,88g
Đặt số mol Al ban đầu là x, số mol Fe phản ứng là y, ta có hệ phương trình:
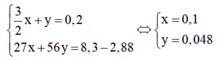
⇒ m A l = 0,1.27 = 2,7g
⇒ % m A l = 2,7/8,3.100 = 32,53%
⇒ Chọn A.

Đặt \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Fe_2O_3}=y\left(mol\right)\end{matrix}\right.\Rightarrow56x+160y=4,8\left(1\right)\)
\(PTHH:Fe+CuSO_4\rightarrow FeSO_4+Cu\\ \Rightarrow n_{Cu}=n_{Fe}=a\left(mol\right)\\ Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\\ Cu+2FeCl_3\rightarrow CuCl_2+2FeCl_2\\ \Rightarrow n_{Cu}=\dfrac{1}{2}n_{FeCl_3}=n_{Fe_2O_3}=b\left(mol\right)\\ \Rightarrow n_{Cu\left(dư\right)}=a-b=\dfrac{3,2}{64}=0,05\left(mol\right)\left(2\right)\)
\(\left(1\right)\left(2\right)\Rightarrow\left\{{}\begin{matrix}a=\dfrac{8}{135}\\b=\dfrac{1}{108}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}\%_{Fe}=\left(\dfrac{8}{135}\cdot56\right):4,8\cdot100\%\approx69,14\%\\\%_{Fe_2O_3}\approx30,86\%\end{matrix}\right.\)
\(b,n_{HCl}=6n_{Fe_2O_3}=\dfrac{1}{18}\approx0,06\left(mol\right)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,06}{1}=0,06\left(l\right)\)

phương trình phản ứng
FeO + H2 = Fe + H2O (1)
y y mol
Fe2O3 + 3H2 = 2Fe + 3H2O (2)
z 2z mol
Fe + CuSO4(dung dịch pha loãng) = FeSO4 + Cu↓ (3)
x x mol
theo phương trình phản ứng (3) áp dụng định luật thay đổi khối lhuowngj ta có 64x - 56x = 4,96 - 4,72 => x=0,03 mol
khối lượng của Fe là mFe = 0,03.56=1,68(g)
khối lượng của oxit sắt còn lại là 3,04 g
theo bài ra ta có phương trình
72y + 160z = 3,04
56y + 56.2z = 3,92 - 1,68
giải hệ phương trình ta có y= 0,02 z= 0,01
còn lại khối lượng bạn tự tính nha![]()

\(PT:Fe+Cu3O_4\rightarrow FeSO_4+Cu\)
\(m\uparrow=-mFe+mCu=4\left(g\right)\)
\(nFe=\dfrac{4}{-56+64}=0,5\left(mol\right)\)
\(\Rightarrow mFe=28\left(g\right)\Rightarrow mCu=72\)

- Độ tăng khối lượng=22-20=2g
Fe+CuSO4\(\rightarrow\)FeSO4+Cu
Gọi số mol Fe=x\(\rightarrow\)số mol Cu=xmol
64x-56x=2 hay 8x=2 suy ra x=0,25mol
mFe=0,25.56=14g\(\rightarrow\)\(m_{Fe_2O_3}=20-14=6g\)
%Fe=\(\dfrac{14.100}{20}=70\%\)
%Fe2O3=30%