Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{HCl}=Cm.V=1.0,1=1mol\)
\(n_{H_2SO_4}=Cm.V=0,5.0,1=0,05mol\)
Thể thích của dd D là 200ml = 0,2l
\([H^+]=\frac{n_{HCl}+2.n_{H_2SO_4}}{V}=\frac{0,1+0,1}{0,2}=1M\)
\([Cl^-]=\frac{n_{HCl}}{V}=\frac{0,1}{0,2}=0,5M\)
\([SO_4^{2-}]=\frac{n_{H_2SO_4}}{V}=\frac{0,05}{0,2}=0,25M\)
Khi cho dd D vào \(Ba\left(OH\right)_2\) chỉ có \(H_2SO_4\) tác dụng, tạo kết tủa
\(H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
\(0,05....\rightarrow0,05mol\)
\(\rightarrow m_{BaSO_4}=n.M=0,05.233=11,65g\)

Đáp án D
VX = 0,3 lit
=> Thể tích mỗi dung dịch axit thành phần là 0,1 lit
=> nH+ = nHCl + 2nH2SO4 + 3nH3PO4 = 0,1.0,3 + 2.0,1.0,2 + 3.0,1.0,1 = 0,1 mol
Để trung hòa thì : nH+ = nOH- = 0,1 mol
Có : nOH- = nNaOH + 2nBa(OH)2 = (0,2 + 0,1.2).V.10-3 = 0,1 mol
=> V = 250 ml

Đáp án D
Ta có n O 2 = 0,05 mol; nNaOH = 0,2. 2 = 0,4 mol
Đặt nCO = x mol; nNO = y mol
→ M X ¯ = m h h n h h = 28 x + 30 y x + y = 14 , 5 . 2 = 29
→x - y = 0 (1)
2CO + O2 → 2CO2
2NO+ O2 →2 NO2
Theo 2 PTHH trên ta có:
n O 2 = 0,5. (nCO + nNO) = 0,5.(x+y) = 0,05 mol (2)
Từ (1) và (2) ta có x = y = 0,05 mol
→Hỗn hợp khí Y có 0,05 mol CO2 và 0,05 mol NO2
Cho Y vào dung dịch NaOH ta có:
CO2+ 2NaOH → Na2CO3+ H2O
0,05 → 0,1
2NO2+ 2NaOH → NaNO2+ NaNO3+ H2O
0,05 0,05
Tổng số mol NaOH phản ứng là 0,1+ 0,05 = 0,15 mol → nNaOH dư = 0,25 mol
Vậy trong dung dịch mới có chứa Na2CO3, NaNO2, NaNO3, NaOH (4 chất tan)

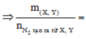
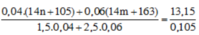

$n_{H_2SO_4} = 0,125.0,2 = 0,025(mol) ; n_{HCl} = 0,25.0,2 = 0,05(mol)$
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
$NaOH + HCl \to NaCl + H_2O$
$n_{NaOH} = 2n_{H_2SO_4} + n_{HCl} = 0,1(mol)$
$\Rightarrow V = \dfrac{0,1}{0,5} = 0,2(lít) = 200(ml)$