Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi
A. Các chất phản ứng phải là những chất dễ tan.
B. Các chất phản ứng phải là những chất điện li mạnh.
C. Một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng
D. Phản ứng không phải là thuận nghịch.

Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi
A. Các chất phản ứng phải là những chất dễ tan.
B. Các chất phản ứng phải là những chất điện li mạnh.
C. Một số ion trong dung dịch kết hợp được với nhau làm giảm nồng độ ion của chúng
D. Phản ứng không phải là thuận nghịch.

\(CH_2=CH-CH_3+H_2O\rightarrow CH_3-CHOH+CH_3\)
\(CH_2=CH-CH_3+H_2O\rightarrow CH_3-CH_2-CH_2OH\)
\(2CH_3-CH_2-CH_2OH\rightarrow CH_3-CH_2-CH_2-O-CH_2-CH_2-CH_3+H_2O\)
Gọi tên : Ete : dipropyl ete.
\(2CH_3-CHOH-CH_3\rightarrow CH_3CH\left(CH_3\right)-O-CH\left(CH_3\right)-CH_3\)
Gọi tên : Ete : disopropylete.
\(CH_3-CH_2-CH_2OH+CH_3-CHOH-CH_3\rightarrow CH_3-CH_2-CH_2-O-CH\left(CH_3\right)-CH_3\)
Gọi tên : Ete : isopropyl propyl ete.
\(CH_3-CH_2-CH_2OH+CuO\rightarrow CH_3-CH_2-CHO+Cu+H_2O\)
\(CH_3-CHOH-CH_3+CuO\rightarrow CH_3-CO-CH_3+Cu+H_2O\)

Phương trình phân tứ và ion xảy ra trong dung dịch :
a) Fe2(SO4)3 + 6NaOH → 2Fe(OH)3\(\downarrow\) + 3Na2SO4
2Fe3+ + 3SO42- + 6Na+ + 6OH- → 2Fe(OH)3\(\downarrow\)+ 6Na+ + 3SO42-
Fe3+ + 3OH- → Fe(OH)3\(\downarrow\)
b) NH4Cl + AgNO3 → NH4NO3 + AgCl↓
NH4 + Cl- + Ag+ + NO3- → NH4+ + NO3- + AgCl↓
Cl- + Ag+ → AgCl↓
c) NaF + HCl → NaCl + HF↑
Na+ + F- + H+ + Cl- → Na+ + Cl- + HF↑
F- + H+ → HF\(\uparrow\)
d) Không có phản ứng xảy ra
e) FeS(r) + 2HCl → FeCl2 + H2S ↑
FeS(r) + 2H+ + 2Cl- → Fe2+ + 2Cl- + H2S↑
FeS(r) + 2H+ \(\rightarrow\) Fe2+ + H2S↑
g) HClO + KOH \(\rightarrow\) KClO + H2O
HClO + K+ + OH- \(\rightarrow\) K+ + CIO- + H2O
HClO + OH- \(\rightarrow\) CIO- + H2O.

Phương trình ion rút gọn :
a) Ca2+ + CO32- → CaCO3 ↓
b) Fe2+ + 2OH- → Fe(OH)2↓
c) HCO3- + H+ → CO2 ↑ + H2O
d) HCO3- + OH- → H2O + CO32-
e) Không có phương trình ion rút gọn.
g) Pb(OH)2(r) + 2H+ → Pb2+ + 2H2O
h) H2PbO2(r) + 2OH- → PbO22- + 2H2O
i) Cu2+ + S2- → CuS↓.

_N2 + 3H2 ---> 2NH3
(bđ)__1____4
(pư)__x____3x______2x
[]____1-x__4-3x_____2x
n(sau) / n(trước) = p(sau) / p(trước) = 0.8 <=> 5 - 2x = 0.8*5 = 4 <=> x = 0.5
=> [N2] = 0.5 / 0.5 = 1(M)
[H2] = 2.5 / 0.5 = 5(M)
[NH3] = 1 / 0.5 = 2(M)
=> Kc = 2^2 : (1 * 5^3) = 0.032
2. pư làm giảm số mol => áp suất giảm theo chiều thuận, tăng theo chiều nghịch
Theo nguyên lí chuyển dịch của lơ-sa-tơ-li-ê, nếu tăng áp suất thì pư sẽ chống lại chiều tăng áp suất tức theo chiều giảm áp suất, tức chiều thuận và ngược lại
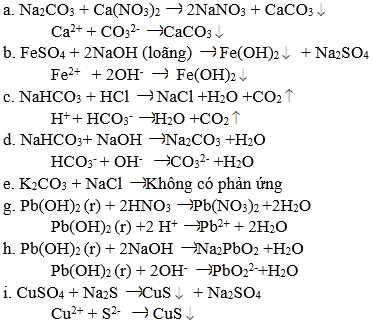
Chọn D