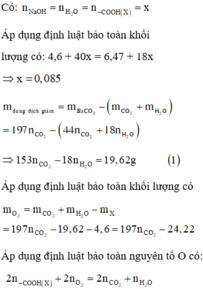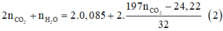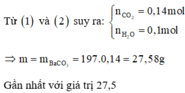Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bảo toàn nguyên tố ta có
\(n_{H_2}=n_{H_2SO_4}=\dfrac{6,72}{22,4}=0.3\) (mol)
Sau khi cô cạn dd ta được : ion kim loại : 11,3g và SO42- 0.3 mol
⇒ m = 30.5 g

nZ = 0,2
Z gồm 2 khí không màu và có MZ = 7,4 ÷ 0,2 = 37
⇒ Trong Z có N2O (VìM = 44 > 37)
+TH1: Z gồm NO và N2O
Đặt nNO =a ; nN2O = b
nZ = a+b = 0,2 (1)
mZ = 30a + 44b = 7,4 (2)
Từ (1) và (2) ⇒ a = b = 0,1
Đặt nNH4+ = x ; nHNO3 ban đầu = y
Ta có nNO3- trong muối kl = ne = 8nN2O + 3n NO + 8nNH4NO3
Bảo toàn nguyên tố N: n HNO3 = n NO3- trong muối kl + n NO + 2nN2O + 2n NH4NO3
⇒ 10x + 4 . 0,1 + 10. 0,1 = y ⇒ 10x + 1,4 = y (*)
m muối = mNH4NO3 + mKL + mNO3-/muối kl
⇒ 80x + 25,3 + (8.0,1 + 3.0,1 + 8x ).62 = 122,3 (**)
Từ (*) và (**) ⇒ nHNO3 ban đầu = y = 1,9
Đáp án C
Tương tự với TH2: Z gồm N2 và N2O, không có đáp án thỏa mãn
Đáp án C.

Đáp án C
Do thu được khí không màu và MZ = 37
⇒ có 2 trường hợp.
TH1: Z gồm N2 và N2O.
Đặt nN2 = x; nN2O = y
⇒ nZ = x + y = 0,2 mol; mZ = 28x + 44y = 7,4(g).
||⇒ giải hệ có: x = 0,0875 mol; y = 0,1125 mol.
Đặt nNH4NO3 = a.
∑nNO3–/KL = ne = 10nN2 + 8nN2O + 8nNH4NO3
= (8a + 1,775) mol.
► mmuối khan = 25,3 + 62.(8a + 1,775) + 80a = 122,3(g)
⇒ a = – 0,02.. ⇒ loại!.
TH2: Z gồm NO và N2O.
Đặt nNO = x; nN2O = y
⇒ nZ = x + y = 0,2 mol; mZ = 30x + 44y = 7,4(g).
⇒ giải hệ có: x = y = 0,1 mol. Đặt nNH4NO3 = a.
∑nNO3–/KL = ne = 3nNO + 8nN2O + 8nNH4NO3 = (8a + 1,1) mol.
► mmuối khan = 25,3 + 62.(8a + 1,1) + 80a
= 122,3(g) ⇒ a = 0,05 mol.
⇒ nHNO3 = 4nNO + 10nN2O + 10nNH4NO3 = 1,9 mol

Ag ko tác dụng với HCl nhé :))
và sản phẩm khử của HNO3 dư ko bao giờ là H2
+) Xét phản ứng với HCl
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Bảo toàn electron: \(2n_{Mg}=2n_{H_2}\) \(\Rightarrow n_{Mg}=0,15\left(mol\right)\)
+) Xét phản ứng với HNO3
Ta có: \(n_{NO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Bảo toàn electron: \(2n_{Mg}+n_{Ag}=n_{NO_2}\) \(\Rightarrow n_{Ag}< 0\)
*Bạn xem lại đề !!