Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Gọi công thức X là CxHyO2
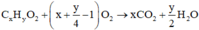
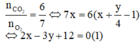
TH1: Nếu X có 1 liên kết π → y = 2x || Từ (1) => x = 3 => y = 6
TH2: Nếu X có 2 liên kết π → y = 2x - 2 || Từ (1) => x = 4,5 (loại) → X là C3H6O2
![]()
+ R = 1 → nKOH pu = 0,18 > 0,14 → loại.
+ R = 15 → nKOH pu = 0,12 mol → m = 0,12 x 74 = 8,88 gam

Giải thích: Đáp án B
mG = 23,02 + 0,46.40 – 0,46.18 = 33,14g
mO2 cần đốt cháy = 0,23.106 + 22,04 – 33,14 = 13,28g
=> nO2 = 0,415 mol
Bảo toàn O : nH2O + 2nCO2 = 1,06 mol
mCO2 + mH2O = 22,04g
=> nCO2 = 0,37 ; nH2O = 0,32 mol
Số C trung bình = (0,37 + 0,23)/0,46 = 1,3 => Y là HCOOH và Z là CH3COOH
=> nX = nCO2 – nH2O = 0,05 mol
=> Tổng số mol của Y và Z là 0,41 mol
0,41 < nCO2(Y,Z) < 0,41.2 = 0,82 mol
Nếu X có 3C => nCO2(Y,Z) = 0,45 mol (thỏa mãn)
Nếu X có 4C trở lên => nCO2(Y,Z) < 0,4 mol (không thỏa mãn)
=> X là C2H3COOH
Đặt nHCOOH = x ; nCH3COOH = y mol
=> x + 2y = 0,6 – 0,05.3
Và x + y = 0,41 mol
=> x = 0,37 ; y = 0,04 mol
=> mZ = 2,4g

Chọn đáp án B.
13,12 gam E + 0,2 mol KOH (vừa đủ) → … -COOK + … nên ∑nO trong E = 0,4 mol.
Giải đốt 13,12 gam E (gồm C, H, O) cần 0,5 mol O2 thu được x mol CO2 + y mol H2O.
12x + 2y +0,4x16 = 13,12
2x+y = 0,4 + 0,5x2
→x = 0,49; y = 0,42
Mặt khác, 0,36 mol E phản ứng vừa đủ với 0,1 mol Br2 và kết hợp giả thiết “chữ” về X, Y.
→ trong hai axit X và Y thì có một axit no và một axit không no, có đúng một nối đôi C=C.
Phản ứng tạo este: 1X + 1Y + 1C2H4(OH)2 → 1Z + 2H2O.
→ Quy đổi E: axit – este về a mol CnH2nO2 + b mol CmH2m-2O2 +c mol 1C2H4(OH)2 – 2c mol H2O.
Ta có tương quan đốt có: ∑nCO2 - ∑nH2O = b + 2c c = b +c = 0,49 -0,42 = 0,07 mol (1).
Bảo toàn nguyên tố oxi có: 2a + 2b =0,4 mol → a + b = 0,2 mol (2).
giả sử tỉ lệ 0,36 mol E so với 13,12 gam E là k, ta có: nE = ka + kb + kc -2kc = 0,36 mol.
Chỉ có kb mol CmH2m-2O2 phản ứng với Br2 → kb = 0,1 mol.
Theo đó, rút gọn k có phương trình: a + b –c =3,6b ↔ 0,2 – c =3,6b (3).
Giải hệ (1), (2), (3) được a = 0,15 mol; b = 0,05 mol; c = 0,02 mol.
Thay lại, có số mol CO2 : 0,15n + 0,05m + 0,02x2 = 0,49↔ 3n + m = 9
Với điều kiện n, m nguyên và yêu cầu n≥1; m≥3→ cặp (n;m) = (2;3) duy nhất thỏa mãn.
Vậy hỗn hợp F gồm 0,15 mol CH3COOK (muối A) và 0,05 mol C2H3COOK (muối B).
→ Tỉ lệ cần tìm a:b = 0,15x98: (0,05x110) ≈ 2,67

Đáp án A
· 13,12 gam E + 0,2 mol KOH (vừa đủ) ® ...-COOK + ... nên ∑nO trong E = 0,4 mol.
Giải đốt 13,12 gam E (gồm C, H, O) cần 0,5 mol O2 thu được x mol CO2 + y mol H2O.
12x + 12y +0,4x16 = 13,12
2x + y = 0,4 +0,5x2
→x = 049; y= 0,42
· Mặt khác, 0,36 mol E phản ứng vừa đủ với 0,1 mol Br2 và kết hợp giả thiết “chữ” về X, Y.
® trong hai axit X va Y thì có một axit no và một axit không no, có đúng một nối đôi C=C.
Phản ứng tạo este: 1X + 1Y + 1C2H4(OH)2 ® 1Z + 2H2O.
® Quy đổi E: axit – este về a mol CnH2nO2 + b mol CmH2m – 2O2 + c mol C2H4(OH)2 – 2c mol H2O.
Ta có tương quan đốt có: ∑nCO2 -∑nH2O = b+ 2c –c =b +c = 0,49-0,42 = 0,07 mol
Bảo toàn nguyên tố oxit có: 2a + 2b = 0,4 mol ® a + b = 0,2 mol (2).
· Giả sử tỉ lệ 0,36 mol E so với 13, 12 gam E là k, ta có: nE = ka + kb + kc – 2kc = 0,36 mol.
Chỉ có kb mol CmH2m – 2O2 phản ứng với Br2 ® kb = 0,1 mol.
Theo đó, rút gọn k có phương trình: a + b – c = 3,6b Û 0,2 – c = 3,6b (3).
Giải hệ (1), (2), (3) được a = 0,15 mol; b = 0,05 mol; c = 0,02 mol.
Thay lại, có số mol CO2: 0,15n + 0,05 + 0,02x2 = 0,49 ↔ 3n+m = 9
Với điều kiện n, m nguyên và yêu cầu n≥1; m≥3 ® cặp (n;m) = (2;3) duy nhất thỏa mãn.
Vậy hỗn hợp F gồm 0,15 mol CH3COOK (muối A) và 0,05 mol C2H3COOK (muối B).
® Tỉ lệ cần tìm a:b = 0,15x98 : (0,05x110) ≈2,67


→ C = 0,49: 0,18 = 2,72.
⇒ X là CH3COOOH:0,13 mol , Y là RCOOH: 0,03 mol , Z là CH3COOCH2-CH2OOCR: 0,02 mol

= 27 (CH2=CH–)
Vậy sau phản ứng thủy phân với KOH thu được ( 0,13+ 0,02) mol CH3COOK và ( 0,03 + 0,02) mol C2H3COOK
→ a : b = (0,15.98) : (0,05. 110) = 2,67

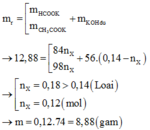
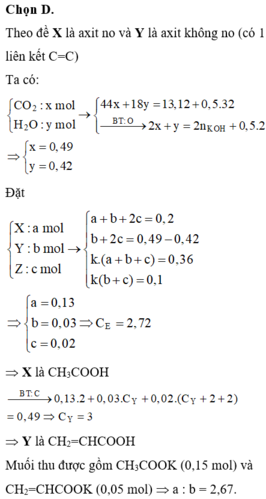
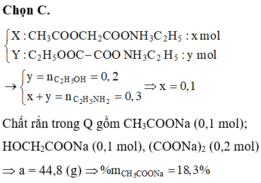


Giải thích: Đáp án C.
17,08 gam axit cacboxylic X + 0,14 mol KOH, 014 mol KOH
Áp dụng bảo toàn khối lượng có:
A đúng. Phương trình phản ứng:
B đúng.
C sai. Trong phân tử chất X có tổng liên kết σ là 6 và có tổng liên kết π là 3.
D đúng. Phương trình phản ứng cháy: