Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nH2(ĐKTC) = 6,72:22,4 = 0,3 (mol)
Khi cho Fe và Al pư với dd NaOH chỉ có Al tham gia pư
Al + NaOH + H2O → NaAlO2 + 3/2H2↑
0,2 ← 0,3 (mol)
=> nAl = 0,2 (mol) => mAl = 0,2.27 = 5,4 (g)
=> mFe = 13,8 – 5,4 = 8,4 (g)
%Fe = (8,4: 13,8).100% = 60,87%

Đáp án C
+ S ơ đ ồ p h ả n ứ n g : B a : x m o l A l F e : y m o l ⏟ m X = 9 , 61 g a m → H 2 ↑ : 0 , 12 m o l A l d ¨ o : y m o l F e : z m o l ⏟ h ỗ n h ợ p Y C u ↓ : 0 , 11 m o l B a ( A l O 2 ) 2 : x + B T E c h o ( 1 ) : 2 n B a ⏟ x + 3 n A l p ¨ o ⏟ 2 x = 2 n H 2 ⏟ 0 , 12 ⇒ x = 0 , 03 . + m Y = m X - m B a - m A l p ¨ o B T E c h o ( 2 ) : 3 n A l + 2 n F e = 2 n C u ⇒ 27 y + 56 z = 3 , 88 3 y + 2 z = 0 , 11 . 2 ⇒ x = 0 , 04 y = 0 , 05 ⇒ % m A l = 27 ( 0 , 06 + 0 , 04 ) 9 , 61 = 28 , 09 %

Đáp án C
Ta có: nCu(NO3)2 = 0 , 2 m o l ; n A g N O 3 = 0 , 1 m o l
Ta có: 0,2.64 + 0,1.108 = 23,6 < 24,16 chứng tỏ Cu(NO3)2 và AgNO3 hết, còn kim loại dư.
Dung dịch Y tác dụng với HCl dư thu được 0,01 mol NO chứng tỏ Y chứa 0,03 mol Fe(NO3)2.
Bảo toàn điện tích: n Mg (NO 3 ) 2 = 0 , 2 . 2 + 0 , 1 - 0 , 03 . 2 2 = 0 , 22 m o l
Mặt khác do Y chứa Fe(NO3)2 nên kim loại chỉ có Fe dư và khối lượng Fe dư là 0,56 gam.
→ m x = 0 , 56 + 0 , 03 . 56 + 0 , 22 . 24 = 7 , 52 → %Fe = 29,79%

Chọn D
Đáp án A sai, vì lượng Fe tạo thành nếu cho tiếp H 2 S O 4 dư vào thì Fe bị hòa tan hết.
Đáp án B sai, vì C u S O 4 sẽ phản ứng hết với Mg và Fe dẫn đến chỉ thu được kim loại Cu.
Đáp án c sai, vì A g N O 3 sẽ phản ứng hết với Mg và Fe dẫn đến chỉ thu được Ag và AgI.
Đáp án D đúng, vì khi Z n 2 + dư loại hết Mg ra thì Zn tiếp tục bị hòa tan bới NaOH thu được Fe
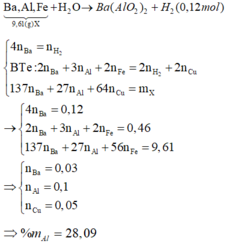



Đáp án A
Theo bài ra ta có:
56nFe + 64nCu =15,2
(Khối lượng ban đầu)
Lại có 3nFe + 2nCu = 0,3.2
(Bảo toàn e)
nFe = 0,1; nCu = 0,15
%mFe = 36,84%; %mCu = 63,16%.