K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Các câu hỏi dưới đây có thể giống với câu hỏi trên

26 tháng 9 2017
Đáp án B
Hỗn hợp khí Y có số mol là 0,14 mol và có M Y = 20 do vậy ta giải được số mol N2O và H2 lần lượt là 0,06 và 0,08 mol.
Khi tác dụng với lượng tối đa NaOH thì kết tủa ta thu được chỉ có Mg(OH)2 nung kết tủa thu được chất rắn là MgO → n M g O = 0 , 24 m o l
Gọi số mol AlCl3 trong dung dịch là a mol , NaCl là b mol, NH4Cl là c mol và MgCl2 là 0,24 mol.

13,52+85b+1,08.36,5 = 133,5a+58,5b+53,5c+0,24.95+0,06.44+0,08.2+18.(0,46-2c)
Giải hệ: a = 0,16; b = 0,1; c = 0,02.
Bảo toàn O:
![]()
![]()







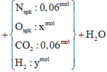






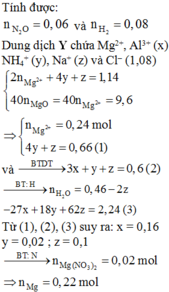
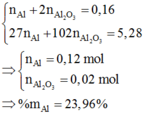

Chọn C
Đặt nH2SO4 = 19x và nNaNO3 = x
Khi cho dd Y tác dụng với NaOH, lọc bỏ kết tủa thì phần nước lọc chứa Na+ : x + 0,444 ( mol) và SO42- : 19x (mol)
Bảo toàn điện tích => x + 0,444 = 19x. 2
=> x = 0,012 (mol)
Trong khí Z đặt a,b,c là số mol NO, CO2, NO2
∑ nZ = a + b + c = 0,11 (1)
∑ mZ = 30a + 44b + 46c = 0,11. 2. 239/11 (2)
Bảo toàn nguyên tố N ∑ nNaNO3 = a + c = 0,012 (3) ( Vì Y + NaOH dư không tạo khí => không tạo muối amoni)
Từ (1), (2), (3) => a= 0,00525 ; b = 0,098; c = 0,00675 (mol)
Bảo toàn electron:
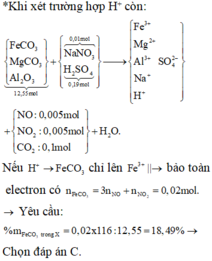
nFeCO3 = 3nNO + nNO2 = 0,0225 (mol)
=> % FeCO3 =[ (0,0225.116): 13,8335].100% = 18,87% ( gần nhất với 20,3%)