Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ca2+ + CO32- → CaCO3 → CaO
nCa2+ = nCaO = 0,28/56 = 0,005 => [Ca2+] = 0,005/0,01 = 0,5M

Đáp án C
Ta có quá trình biến đổi nhau sau:
CaCO3 → CaO.
⇒ Rắn đó là CaO
⇒ nCaO = 0,005 mol = nCa2+
Û CM Ca2+ = 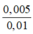 = 0,5M
= 0,5M

Đáp án A
Ca2+ + CO32- → CaCO3↓
CaCO3 → t o CaO + CO2 ↑ (nCaO = 0,28: 56 = 0,005 mol)
=> nCa2+ = nCaCO3 = nCaO = 0,005 mol
=> CM (Ca2+) = 0,005: 0,01 = 0,5M

Đáp án : A
Ta thấy chất rắn D gồm toàn oxit của Mg (và có thể của Fe) có m < mA
=> chứng tỏ A không phản ứng hết mà có kim loại dư.
Giả sử Fe chỉ phản ứng 1 phần với số mol là x; nMg = y
=> CuSO4 hết
=> moxit = mMgO + m F e 2 O 3 = 40y + 80x = 0,9g
Lại có : mB – mA = mCu – mMg – mFe pứ
=> 1,38 – 1,02 = 64.(x + y) – 24y – 56x
=> x = y = 0,0075 mol
=> n C u S O 4 = x + y = 0,015 mol
=> C M C u S O 4 = 0,075M

Đáp án A
Bài này có thể giải theo kinh nghiệm,
hoặc biện luận rào số mol hỗn hợp A.
Từ đó ⇒ giới hạn của chất rắn C
Trường hợp xả ra đó là:
Fe pứ hết và Cu chỉ pứ 1 phần
⇒ C gồm Ag và Cu chưa tan.
+ Sơ đồ ta có:
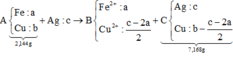

PT theo khối lượng oxit:
40c = 2,56 Û c = 0,064 mol
⇒ CM AgNO3 = 0,064 ÷ 0,2 = 0,32

E nung tạo 2 oxit , Mà A chứa 3 cation => E có 3 hidroxit
A chứa 3 cation => đó là : Fe2+ ;Fe3+;Cu2+. Các phản ứng : Fe + 2Ag+ → Fe2+ + 2Ag
Fe + Cu2+ → Fe2+ + Cu
Fe2+ + Ag+ → Fe3+ + Ag
Để thỏa mãn đề thì Fe2+ phải dư hơn so với Ag+
=> c/3 < a < c/2
=>B
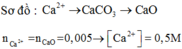
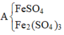
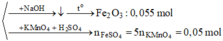

Chọn đáp án D