Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Fe+2HCl\rightarrow FeCl_2+3H_2\\ Đặt:n_{Al}=a\left(mol\right);n_{Fe}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}27a+56b=11\\1,5a+b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\ a,n_{HCl}=2.n_{H_2}=2.0,4=0,8\left(mol\right)\\ \Rightarrow V_{ddHCl}=\dfrac{0,8}{8}=0,1\left(l\right)\\ b,FeCl_2+2AgNO_3\rightarrow Fe\left(NO_3\right)_2+2AgCl\downarrow\\ AlCl_3+3AgNO_3\rightarrow Al\left(NO_3\right)_3+3AgCl\downarrow\\ n_{AgCl}=n_{AgNO_3}=3.n_{AlCl_3}+2.n_{FeCl_2}=3.a+2.b=3.0,2+2.0,1=0,8\left(mol\right)\\ \Rightarrow a=\dfrac{170.0,8}{250}.100=54,4\%\\ b=m_{\downarrow}=m_{AgCl}=0,8.143,5=114,8\left(g\right)\)

Đáp án B
Ta có NaX + AgNO3 → NaNO3 + AgX
M tăng = 108-23 = 85, m tăng = 8,5
nAgX = 0,1, MAgX = 143,5 => X :35,5 (Cl)
Ta có ![]()

Đáp án B
Ta có NaX + AgNO3 → NaNO3 + AgX
M tăng = 108-23 = 85, m tăng = 8,5
nAgX = 0,1, MAgX = 143,5 => X :35,5(Cl)
ta có: ![]() = 35,5 => x = 75%
= 35,5 => x = 75%

Đáp án B
Khi cho NaX vào AgNO3 thu được kết tủa là AgX
Luôn có:
n NaX = n AgX ⇒ 5 , 85 23 + M X = 14 , 35 108 + M X ⇒ M X = 35 , 5
Ta có hệ
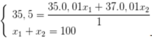
⇒


Chất rắn k tan là Cu và có KL là 1g
\(Fe2O3+6HCl-->2FeCl3+3H2O\)
\(FeCl3+3NaOH-->Fe\left(OH\right)3+3NaCl\)
\(2Fe\left(OH\right)3-->Fe2O3+3H2O\)
\(n_{Fe2O3}=\frac{32}{160}=0,2\left(mol\right)\)
\(n_{Fe\left(OH\right)3}=2n_{Fe2O3}=0,4\left(mol\right)\)
\(n_{FeCl3}=n_{Fe\left(OH\right)3}=0,4\left(mol\right)\)
\(n_{Fe2O3}=\frac{1}{2}n_{FeCl3}=0,2\left(mol\right)\)
\(m_{Fe2O3}=0,2.160=32\left(g\right)\)
\(m=mFe2O3+m_{Cu}=32+1=33\left(g\right)\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(2FeCl_3+Cu\rightarrow CuCl_2+2FeCl_3\)
\(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
\(4Fe\left(OH\right)_2+2H_2O+O_2\rightarrow4Fe\left(OH\right)_2\)
\(Cu\left(OH\right)_2+CuO+H_2O\)
\(2Fe\left(OH\right)_3\rightarrow Fe_2O_3+3H_2O\)
\(a:Fe_2O_3\)
\(\Rightarrow n_{Cu_{pư}}=0,5a\left(mol\right)\)
\(160a+0,5a.80=32\)
\(\Rightarrow a=0,16\left(mol\right)\)
\(m_{Fe2O3}=0,16.160=25,6\)
\(m_{Cu}=0,08.64+1=6,12\left(g\right)\)
\(\Rightarrow m=25,6+6,12=31,72\left(g\right)\)
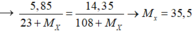
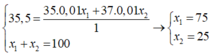

\(HCl + AgNO_3 \to AgCl + HNO_3\\ n_{HCl} = n_{AgCl} = \dfrac{14,35}{143,5} = 0,1(mol)\\ \Rightarrow C\%_{HCl} = \dfrac{0,1.36,5}{10}.100\% = 36,5\%\)