Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo đề bài: cho A phản ứng với dung dịch NaOH thu được glixerol và 2 muối của 2 axit đơn chức, A chỉ chứa 1 loại nhóm chức
=> A là este 3 chức phản ứng với NaOH theo tỷ lệ mol 1:3 tạo ra 0,02 mol glixerol nên tiêu thụ 0,06 mol NaOH, tạo ra 0,04 mol 1 muối và 0,02 mol muối còn lại.
A + 3NaOH → C3H5(OH)3 + 2R1COONa + R2COONa
0,06 ← 0,02 → 0,04 → 0,02
=> nNaOH dư = 0,025.4 – 0,06 = 0,04 mol
Ta lại có: Axit X ít hơn Y 2 nguyên tử C và có cùng số nguyên tử H.
=> Gọi CTPT của các muối của X, Y với số mol tương ứng là CnHmCOONa x mol và Cn+2HmCOONa y mol.
Bảo toàn Na ta có:
nNa2CO3 = 1/2nNaOH bđ = 0,05 mol
Dẫn hỗn hợp khí và hơi sau khi đốt cháy B vào dung dịch Ba(OH)2 dư thì xảy ra phản ứng: Ba(OH)2 + CO2 → BaCO3 + H2O
=> nCO2 = nBaCO3 = 195,03/197 = 0,99 mol
Bảo toàn C ta có (n+1)x + (n+3)y = 0,05 + 0,99 =1,04 (*)
Xét 2 trường hợp có thể có với este A.
Trường hợp 1: A chứa 2 gốc axit X và 1 gốc axit Y
=> x = 0,04 mol, y = 0,02 thay vào (*) thì n = 15,67 vô lí (loại).
Trường hợp 2: A chứa 2 gốc axit Y và 1 gốc axit X
=> x = 0,02 mol, y = 0,04 mol thay vào (*) thì n =15
Khi đó 19,24 gam hỗn hợp B gồm: C15HmCOONa 0,02 mol, C17HmCOONa 0,04 mol và NaOH dư 0,04 mol.
=> 0,02(247 + m) + 0,04(271 + m) + 0,04 . 40 = 19,24
=> m = 31 (thỏa mãn)
=> 2 muối thu được là C15H31COONa và C17H31COONa
Este A có dạng:
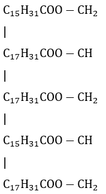
CTPT của A là C55H98O6

nH2 = 85,12 : 22,4 = 3,8 (mol) ; nH2O = VH2O.D = 108 (g) => nH2O = 108/18 = 6 (mol)
PTHH:
2Na + 2C2H5OH → 2C2H5ONa + H2↑
x → 0,5x (mol)
2Na + 2H2O → 2NaOH + H2↑
6 → 3 (mol)
Ta có: nH2 = 0,5x + 3 = 3,8
=> x = 1,6 (mol) = nC2H5OH
mC2H5OH = 1,6.46 = 73,6 (g)
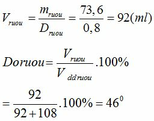

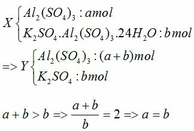
Vì dung dịch sau phản ứng chỉ chứa một chất tan => Z chỉ chứa KAlO2 hoặc K2SO4.
Khi cho từ từ Ba(OH)2 vào Y thì có thể xảy ra các phản ứng:
Al2(SO4)3 + 3Ba(OH)2 → 2Al(OH)3 + 3BaSO4(1)
2b → 6b 4b 6b (mol)
K2SO4 + Ba(OH)2 → 2KOH + BaSO4 (2)
b → b 2b b (mol)
Al(OH)3 + KOH → KAlO2 + 2H2O (3)
2b →2b 2b (mol)
· Trường hợp 1: Chất tan trong Z là K2SO4 → vừa đủ phản ứng (1)
Theo đề => a= b = 0,02 mol
nBaSO4 = nBa(OH)2 = 6b = 0,12mol
nAl(OH)3 = 4b = 0,08mol
m1= 948 . 0,02 + 342 . 0,02 = 25,8 gam
m2 = 0,08 . 78 + 0,12 . 233 = 34,2 gam
V = 0,12/2 = 0,06 lít = 60ml
· Trường hợp 2: Chất tan trong Z là KAlO2 →xảy ra cả (1,2,3)
nKAlO2 = 0,02mol
=> 2b = 0,02 => a = b =0,01
nBaSO4 = nBa(OH)2 = 7b = 0,07
nAl(OH)3 = 4b – 2b = 0,02
=> m1= 948.0,01 + 342.0,01 = 12,9 gam
m2 = 0,02.78 + 0,07.233 = 17,87 gam
V = 0,07/2 = 0,035 lít = 35ml



Ba+2H2O\(\rightarrow\)Ba(OH)2+H2
2Na+2H2O\(\rightarrow\)2NaOH+H2
nH2=0,03\(\rightarrow\)nOH-=0,06
Gọi số mol Ba và Na là a
Ta có \(\text{nH2=nBa+0,5nNa=a+0,5a=0,03}\)
\(\rightarrow\)a=0,02
nAl2(SO4)3=0,02\(\rightarrow\)nAl3+=0,04
nSO42-=0,06
Al3+ +3OH- \(\rightarrow\)Al(OH)3
Để d cực đại thì Al3+ bị kết tủa hết và không bị hòa tan
\(\rightarrow\)nOH-=3nAl3+=0,12
\(\rightarrow\)nOH- cần thêm là \(\text{0,12-0,06=0,06}\)
\(\rightarrow\)mNaOH=2,4g
tính giùm mình lượng kết tủa cực đại luôn nhé