Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Có quá trình khử : 4H+ + NO3- + 3e → NO +2H2O
Có nH+ = 1 mol, nNO3- = 0,6 mol ⇒ số e nhận tối đa là 3 × 1 ÷ 4 = 0,75 mol
Quá trình oxi hoá : Cu → Cu2+ + 2e và Fe2+ → Fe3+ + 1e
Số e nhường tối đa là là 2×0,15 + 0,3 = 0,6 mol < ne nhận tối đa
Vậy chứng tỏ NO được tính theo số e nhường ⇒ NO = 0,6 : 3 = 0,2 mol.
⇒ V = 4,48 lít
Đáp án là B

Đáp án B
Có quá trình khử : 4H+ + NO3- + 3e → NO +2H2O
Có nH+ = 1 mol, nNO3- = 0,6 mol ⇒ số e nhận tối đa là 3 × 1 ÷ 4 = 0,75 mol
Quá trình oxi hoá : Cu → Cu2+ + 2e và Fe2+ → Fe3+ + 1e
Số e nhường tối đa là là 2×0,15 + 0,3 = 0,6 mol < ne nhận tối đa
Vậy chứng tỏ NO được tính theo số e nhường ⇒ NO = 0,6 : 3 = 0,2 mol.
⇒ V = 4,48 lít

3Cu+ 8H+ +2NO−3−−−>3Cu2+ + 2NO + H2O ( *)
0,3 ----- 1,8 ----- 1,2 -----------0,3-----0,2 --- mol
Cu2+ +2Fe2+−−−> 2Fe3+ +Cu
0,3 ------- 0,6 --------------------0,3
3Cu + 8H+ +2NO−3 −−−> 3Cu2+ +2NO + H2O ( ** )
0,3 ----- 1,8 ----- 1,2 -----------0,3-----0,2 --- molTừ (*) và (**) ==> n NO = 0,4 mol
=> V = 8,96 mol
=> Đáp án B

Đáp án : D
3Cu + 8H+ + 2NO3- -> 3Cu2+ + 2NO + 4H2O
Cu + 2Fe3+ -> Cu2+ + 2Fe2+
Dựa vào 2 phản ứng trên
=> Dung dịch sau phản ứng có : 0,06 mol Fe2+ ; 0,21 mol Cu2+ ; 0,06 mol NO3- ; 0,24 mol SO42-
=> mmuối = 43,56g

Đáp án B
Quy đổi hỗn hợp về Fe và O. Đặt nFe = a và nO = b
+ Vì HNO3 dư và nFe(NO3)3 = 0,4 mol ⇒ nFe = a = 0,4 mol
+ Áp dụng bảo toàn e ta có: 3nFe = 2nO + 3nNO
⇒ nO = 0,3 mol ⇒ m = 0,4×56 + 0,3×16 = 27,2 gam

Đáp án là B.
Sau phản ứng thu được hỗn hợp kim loại nên Fe dư.
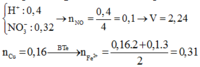
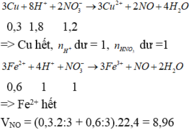

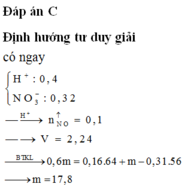
Đáp án B