Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

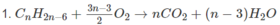
Cứ ( 14n - 6) g A tạo ra n mol C O 2
Cứ 1,50 g A tạo ra 
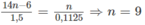
Công thức phân tử của A là C 9 H 12
2. Các công thức cấu tạo
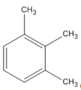 (1,2,3-trimetylbenzen )
(1,2,3-trimetylbenzen )
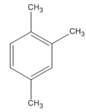 (1,2,4-trimetylbenzen)
(1,2,4-trimetylbenzen)
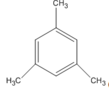 (1,3,5-trimetylbenzen)
(1,3,5-trimetylbenzen)
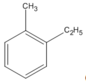 (1-etyl-2-metylbenzen)
(1-etyl-2-metylbenzen)
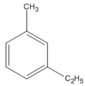 (1-etyl-3-metylbenzen)
(1-etyl-3-metylbenzen)
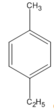 (1-etyl-4-metylbenzen)
(1-etyl-4-metylbenzen)
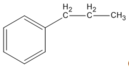 (propylbenzen)
(propylbenzen)
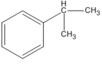 (isopropylbenzen)
(isopropylbenzen)
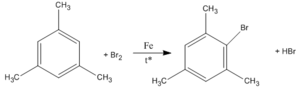
3. 

1. Theo định luật bảo toàn khối lượng:
m A = m C O 2 + m H 2 O − m O 2
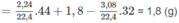
Khối lượng C trong 1,8 g A là: 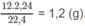
Khối lượng H trong 1,8 g A là: 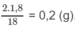
Khối lượng O trong 1,8 g A là : 1,8 - 1,2 - 0,2 = 0,4 (g).
Công thức chất A có dạng C x H y O z :
x : y : z = 0,1 : 0,2 : 0,025 = 4 : 8 : 1
CTĐGN là C 4 H 8 O
2. M A = 2,25.32 = 72 (g/mol)
⇒ CTPT trùng với CTĐGN: C 4 H 8 O .
3. Các hợp chất cacbonyl C 4 H 8 O :
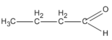 (butanal)
(butanal)
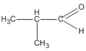 (2-metylpropanal)
(2-metylpropanal)
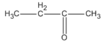 (butan-2-ol)
(butan-2-ol)

a)
Gọi CT của ankan là CnH2n+2
CnH2n+2 + O2 \(\underrightarrow{t^o}\) nCO2 + (n+1)H2O
Theo đầu bài ta có: mCO2 + mH2O = 20,4
n = 3
Vậy CTPT của X là C3H8. …
Vì hỗn hợp Z tác dụng với dung dịch AgNO3/NH3 thu được kết tủa \(\rightarrow\) hiđrocacbon B có liên kết 3 đầu mạch.
Gọi CTTB của 2 hidrocacbon A và B là \(C_{\overline{x}}H_{\overline{y}}\)
\(C_{\overline{x}}H_{\overline{y}}\) + O2 \(\rightarrow\overline{x}\)CO2 + \(\frac{\overline{y}}{2}\)H2O
Theo đề bài ta có \(\overline{x}\) = 2,6 (vì \(\overline{x}\) = 2,6 nên hiđroccacbon B có số nguyên tử nhỏ hơn 2,6).
Vậy hiđrocacbon B là C2H2
Gọi \(n_{C_2H_2}=x,\) \(n_{C_3H_8}=y\) .Ta có: \(\begin{cases}x+y=0,1\\2x+3y=0,26\end{cases}\)\(\rightarrow\begin{cases}x=0,04\\y=0,06\end{cases}\)
Khối lượng kết tủa là C2Ag2 m = 9,6 gam

1. Khi đun nóng A có mặt chất xúc tác Ni, chỉ còn lại 1 chất khí duy nhất. Vậy ankan và anken trong A có cùng số nguyên tử cacbon.
Giả sử trong 100 ml A có x mol C n H 2 n + 2 ; y mol C n H 2 n và z mol H 2 .
x + y + z = 100 (1)
Khi đốt cháy hoàn toàn 100 ml A :
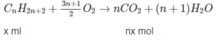
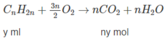
2 H 2 + O 2 → 2 H 2 O
Thể tích C O 2 : n(x + y) = 210 (2)
Khi đun nóng A có mặt chất xúc tác Ni:
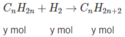
x + y = 70 (3)
y = z (4)
Giải hộ phương trình, tìm được n = 3; x = 40 ; y = z = 30.
Thành phần thể tích của hỗn hợp A là : C 3 H 8 : 40% ; C 3 H 6 : 30%; H 2 : 30%
2. Thể tích O 2 là 350 ml.

1. CTĐGN là C 7 H 8 O
2. CTPT là C 7 H 8 O
3. Có 5 CTCT phù hợp :
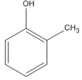 (2-metylphenol (A1))
(2-metylphenol (A1))
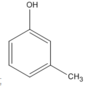 (3-metylphenol (A2))
(3-metylphenol (A2))
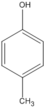 (4-metylphenol (A3))
(4-metylphenol (A3))
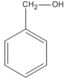 (ancol benzylic (A4))
(ancol benzylic (A4))
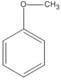 ( metyl phenyl ete (A5))
( metyl phenyl ete (A5))
4. Có phản ứng với Na: A1, A2, A3, A4;
Có phản ứng với dung dịch NaOH: A1, A2, A3.

Giả sử trong 6,72 lít A có x mol C n H 2 n + 2 y mol C m H 2 m - 2 .
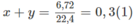
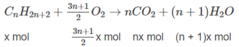
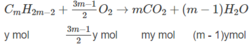
Số mol O 2 :
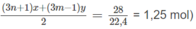
⇒(3n + 1)x + (3m − 1)y = 2,5 (2)
Số mol C O 2 : nx + my = 0,8 (mol)
⇒ (3n + 1)x + (3m - 1)y = 2,5 (3)
Từ (2) và (3) tìm được x - y = 0,1 ;
Kết hợp với X + y = 0,3, ta có: x = 0,2 và y = 0,1 Thay các giá trị tìm được vào (3) ta có
0,2n + 0,1m = 0,8
⇒ 2n + m = 8.
Nếu n = 1 thì m = 6: Loại, vì C 6 H 10 không phải là chất khí ở đktc. Nếu n = 2 thì m = 4. Công thức hai chất là C 2 H 6 và C 4 H 6 .
Nếu n = 3 thì m = 2: Loại vì m > 3.
Trả lời: Hỗn hợp A chứa (66,67%) và C 4 H 6 (33,33%)
Số mol H 2 O = (n + 1)x + (m - 1)y = 0,9 (mol).
2. Khối lượng nước: p = 0,9.18 = 16,2 (g).

Số mol
O
2
: 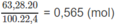
Số mol C O 2 = số mol C a C O 3 = 0,36 (mol).
1. Trong 0,36 mol C O 2 , khối lượng cacbon: 0,36 x 12 = 4,32 (g) và khối lượng oxi: 0,36 x 32 = 11,52 (g).
Khối lượng oxi trong nước là: 0,565 x 32,0 - 11,52 = 6,56 (g).
Khối lương hiđro (trong nước): 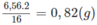
Khối lượng M = khối lượng C + khối lượng H = 4,32 + 0,82 = 5,14 (g)
2. Khi đốt 1 mol ankan, số mol H 2 O tạo ra nhiều hơn số mol C O 2 là 1 mol. Khi đốt hỗn hợp M, số mol H 2 O nhiều hơn số mol C O 2 :
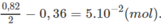
Vậy hỗn hợp M có 5. 10 - 2 mol ankan.
Khối lượng trung bình của 1 mol ankan:
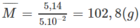
14n + 2 < 102,8 < 14n + 30
⇒ 5,20 < n < 7,20
Đến đây có thể tìm được công thức phân tử và phần trăm khối lượng từng chất như ở cách thứ nhất.
1.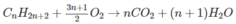
Đối với các chất khí, tương quan về số mol trùng với tương quan vể thể tích. Vì thế từ phương trình hoá học ở trên, ta có :
Cứ 1 lít ankan tác dụng với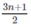 lít
O
2
lít
O
2
Cứ 1,2 lít ankan tác dụng với 6,0 lít O 2 .
⇒ n = 3 ; CTPT chất A là C 3 H 8 .
2.