Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Vì Cu không phản ứng với HCl
=> mCu = 2,54 (g)
=> mMg và Al = 9,14 - 2,54 = 6,6 (g)
nH2 = \(\dfrac{7,84}{22,4}\)= 0,35 (mol)
Gọi x và lần lượt là số mol của Mg và Al
Mg + 2HCl ----> MgCl2 + H2
x x x (mol)
2Al + 6HCl ----> 2AlCl3 + 3H2
y y \(\dfrac{3}{2}\)y (mol)
Theo đề ra, ta có:
24x + 27y = 6,6
x + \(\dfrac{3}{2}\)y = 0,35
=> x = 0,05
y = 0,2
=> mMg = 0,05.24 = 1,2 (g)
=> mAl = 0,2.27 = 5,4 (g)
=> %Cu = \(\dfrac{2,54.100\%}{9,14}\)= 28%
=> %Mg = \(\dfrac{1,2.100\%}{9,14}\)= 13%
=> %Al = 100 - 28 - 13 = 59%
mMgCl2 = 0,05.95 = 4,75 (g)
mAlCl3 = 0,2.133,5 = 26,7 (g)
=> m = 4,75 + 26,7 = 31,45 (g)

a) \(n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,05<-----------0,05---->0,075
=> \(\%Al=\dfrac{0,05.27}{14,15}.100\%=9,54\%\)
=> \(\%Cu=\dfrac{14,15-0,05.27}{14,15}.100\%=90,46\%\)
b) \(V_{H_2}=0,075.22,4=1,68\left(l\right)\)
c) \(n_{Cu}=\dfrac{14,15-0,05.27}{64}=0,2\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,05->0,0375
2Cu + O2 --to--> 2CuO
0,2-->0,1
=> \(V_{O_2}=\left(0,1+0,0375\right).22,4=3,08\left(l\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ m_{AlCl_3}=6,675\left(mol\right)\\ n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\\ \Rightarrow n_{Al}=n_{AlCl_3}=0,05\left(mol\right)\\ \Rightarrow m_A=0,05.27=1,35\left(g\right);m_{Cu}=14,15-1,35=12,8\left(g\right)\\ \%m_{Cu}=\dfrac{12,8}{14,15}.100\approx90,459\%\\ \Rightarrow\%m_{Al}\approx9,541\%\\ b,n_{Cu}=\dfrac{12,8}{64}=0,2\left(mol\right)\\ n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,05=0,075\left(mol\right)\\ \Rightarrow V=V_{H_2\left(đktc\right)}=0,075.22,4=1,68\left(l\right)\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ 2Cu+O_2\rightarrow\left(t^o\right)2CuO\\ n_{O_2}=\dfrac{3}{4}.n_{Al}+\dfrac{1}{2}.n_{Cu}=\dfrac{3}{4}.0,05+\dfrac{1}{2}.0,2=0,0875\left(mol\right)\)
\(\Rightarrow V_{O_2\left(đktc\right)}=0,0875.22,4=1,96\left(l\right)\)

\(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
Chất rắn Y là Cu. Vì Cu đứng sau H trong dãy hđhh
\(m_{Mg}+m_{Al}=9,14-2,54=6,6\left(g\right)\)
Gọi x,y lần lượt là số mol của Mg, Al
Pt: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
x -----------------------------------> x
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
y ------------------------------> 1,5y
Lập hệ => x = 0,05 ; y = 0,2
\(m_{khan}=0,05.95+0,2.133,5=31,45\left(g\right)\)
- Chất rắn là Cu
\(\Rightarrow\) mhỗn hợp Mg và Al = 9,14 - 2,54 = 6,6 (g)
nH2 = 0,35 mol
Đặt nMg = x ; nAl = y ( x , y > 0 )
Mg + 2HCl \(\rightarrow\) MgCl2 + H2
x.........2x.............x............x
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
y........3y............y.............1,5y
Ta có hệ
\(\left\{{}\begin{matrix}24x+27y=6,6\\x+1,5y=0,35\end{matrix}\right.\)
\(\Rightarrow\) \(\left\{{}\begin{matrix}x=0,05\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\) mmuối khan = ( 0,05.95 )+(0,2.133,5) = 31,45 (g)

Đáp án A
Chất rắn Y là Cu không phản ứng
nHCl = ![]() = 2.0,35 = 0,7
= 2.0,35 = 0,7
mmuối = mKL + mgốc axit = (9,14 – 2,54) + 0,7.35,5 = 31,45(g)

\(19,1gam\) \(:\left\{{}\begin{matrix}Al\\Mg\\Zn\end{matrix}\right.\)\(\underrightarrow{+O_2}\)\(Y:25,5gam\)\(\underrightarrow{+HCl}\left\{{}\begin{matrix}AgCl_3\\MgCl_2\\ZnCl_2\end{matrix}\right.\) + H2 : 0,3 mol
H2O
Áp dụng định luật bảo toàn khối lượng:
\(mO_2=25,5-19,1=6,4gam\) \(\Rightarrow nO_2=0,2\left(mol\right)\)
BTNT O : nH2O = 0,4mol
\(\rightarrow nHCl^-\left(tdOxi\right)=0,8\left(mol\right)\)
\(nH_2=0,3\left(mol\right)\rightarrow nCl^-\left(tdKl\right)=0,6\left(mol\right)\)
\(m_{muối}=19,1+\left(0,8+0,6\right).35,5=68,8\left(g\right)\)

Mg + 2 HCl -> MgCl2 + H2
x____2x_______x___x(mol)
2 Al + 6 HCl -> 2 AlCl3 + 3 H2
y____3y_______y____1,5y(mol)
Cu k tác dụng vs dd HCl -> m(rắn)=mCu= 6,4(g)
=> m(Mg, Al)= 10,14- 6,4=3,74(g)
=> \(\left\{{}\begin{matrix}24x+27y=3,74\\22,4x+22,4.1,5y=7,84\end{matrix}\right.\)
giải ra nghiệm âm, em xem lại đề nha!

Gọi số mol Al, Fe là a, b
\(m_{Cu}=m_B=6,4\left(g\right)\)
=> \(m_{Al}+m_{Fe}=17,4-6,4=11\left(g\right)\)
=> 27a + 56b = 11
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
b----------------------->b
2Al + 6HCl --> 2AlCl3 + 3H2
a------------------------>1,5a
=> 1,5a + b = 0,4
=> a = 0,2; b = 0,1
=> \(\left\{{}\begin{matrix}m_{Fe}=0,1.56=5,6\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)
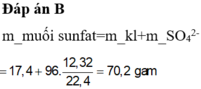
\(m_{hhcl}=9.14-2.54=6.6\left(g\right)\)
\(n_{HCl}=2n_{H_2}=2\cdot\dfrac{7.84}{22.4}=0.7\left(mol\right)\)
\(m_{Muối}=m_{hh}+m_{Cl^-}=6.6+0.7\cdot35.5=31.45\left(g\right)\)