Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tương tự bài 1, ta có:
m 4 o x i t = m m u o i - m H 2 S O 4 + m H 2 O s a n p h a m
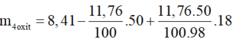
m 4 o x i t = 3,61g
⇒ Chọn C.

nH2= 2.24: 22.4 = 0,1(mol)
nNaAlO2= 16,4:82=0,2(mol)
Gọi nAl=a (mol;a>0)
nNaAlO2= b (mol; b>0)
(1) Al + NaOH + H2O --> NaAlO2 + 3/2 H2
Ta có a a a 1,5a (mol)
(2) Al2O3 + 2NaOH --> 2NaAlO2 + H2O
Ta có b 2b (mol)
Ta có nH2 = 0,1 (mol) => 1,5a = 0,1 => a = 2/30=>nAl = 2/30(mol)
nNaAlO2 = 0,2(mol) =>a+2b=0,2=> b=??
Còn lại bn tự làm nha!!!!!!!!
Có chỗ nào sai mong mọi người thông cảm:))

$n_{HCl} = 0,8.0,5 = 0,4(mol) ; n_{H_2SO_4} = 0,6(mol) ;n_{H_2} = 0,2(mol)$
$n_{H(trong\ axit)} = 0,4 + 0,6.2 = 1,6(mol)$
Bảo toàn H : $n_{H_2O} = \dfrac{n_{H(trong\ axit)} - 2n_{H_2} }{2} = 0,6(mol)$
Bảo toàn khối lượng :
$m = 88,7 + 0,6.18 + 0,2.2 - 0,4.36,5 - 0,6.98 = 26,5(gam)$

a) Gọi \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\left(\text{Đ}K:a,b>0\right)\)
PTHH: Zn + H2SO4 ---> ZnSO4 + H2
a------>a---------->a----------->a
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
b----->1,5b--------->0,5b------->1,5a
=> \(\left\{{}\begin{matrix}65a+27b=20,3\\161b+0,5a.342=65,9\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,25\\b=0,15\end{matrix}\right.\)
=> \(V=V_{H_2}=\left(0,25+0,15.1,5\right).22,4=10,64\left(l\right)\)
b) \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,25.65}{20,3}.100\%=80,05\%\\\%m_{Al}=100\%-80,05\%=19,95\%\end{matrix}\right.\)
c) \(m_{\text{dd}H_2SO_4}=\dfrac{\left(0,25+1,5.0,15\right).98}{10\%}=465,5\left(g\right)\)

Đặt CT chung 3 KL là R có hóa trị chung là n
\(PTHH:4R+nO_2\xrightarrow{t^o}R_2O_n\\ R_2O_n+nH_2SO_4\to R_2(SO_4)_n+nH_2O\\ \Rightarrow n_{H_2SO_4}=n_{H_2O}\\ \text {Bảo toàn KL: }m_{R_2O_n}+m_{H_2SO_4}=m_{R_2(SO_4)_3}+m_{H_2O}\\ \Rightarrow 2,8+98n_{H_2SO_4}=6,8+18n_{H_2SO_4}\\ \Rightarrow n_{H_2SO_4}=0,05(mol)\\ \Rightarrow V=V_{dd_{H_2SO_4}}=\dfrac{0,05}{1}=0,05(l)=50(ml)\\ \text {Ta có: }n_{O_2}=\dfrac{n_{R_2O_3}}{2}.n;n_{R_2O_3}=\dfrac{n_{H_2SO_4}}{n}\\ \Rightarrow n_{O_2}=\dfrac{n_{H_2SO4}}{2}=0,025(mol)\\ \Rightarrow m_{O_2}=0,025.32=0,8(g)\\ \text {Bảo toàn KL: }m=m_R+m_{O_2}=m_{R_2O_n}\\ \Rightarrow m=m_R=2,8-0,8=2(g)\)

`MgCO_3+2HCl->MgCl_2+CO_2+H_2O`
`Mg+2HCl->MgCl_2+H_2`
`FeCO_3+2HCl->FeCl_2+CO_2+H_2O`
Đặt \(\hept{\begin{cases}x\left(mol\right)=n_{H_2}\\y\left(mol\right)=n_{CO_2}\end{cases}}\)
\(\rightarrow2x+44y=4,8\left(1\right)\)
Có \(\overline{M}_B=8.M_{H_2}=16\)
\(\rightarrow n_B=x+y=0,2mol\) và \(y=0,1mol\)
Theo phương trình \(n_{H_2O}=n_{CO_2}=0,1mol\)
BT H \(\text{∑}n_{HCl}=2n_{H_2O}+2n_{H_2}=0,6mol\)
BT khối lượng \(m_A+m_{HCl}=m_{\text{muối}}+m_{CO_2}+m_{H_2O}+m_{H_2}\)
\(\rightarrow m+0,6.36,5=4,8+0,1.18+40,9\)
\(\rightarrow m=25,6g\)
Có; \(n_{NO}+n_{N_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(\dfrac{30n_{NO}+28n_{N_2}}{n_{NO}+n_{N_2}}=\dfrac{43}{3}.2=\dfrac{86}{3}\)
=> nNO = 0,1 (mol); nN2 = 0,2(mol)
Al0 -3e --> Al+3
a-->3a--->a
Mg0 -2e --> Mg+2
b---->2b---->b
Fe0 -3e --> Fe+3
c--->3c---->c
4H+ + NO3- +3e --> NO + 2H2O
0,4<----------0,3<----0,1
12H+ + 2NO3- +10e--> N2 + 6H2O
2,4<---------------2<-----0,2
10H+ + 2NO3- +8e--> NH4NO3 + 3H2O
0,5<-------------0,4<-----0,05
=> nHNO3 = nH+ = 0,4 + 2,4 + 0,5 = 3,3 (mol)
=> \(V_{dd}=\dfrac{3,3}{1}=3,3\left(l\right)\)
Bảo toàn H: \(n_{H\left(HNO_3\right)}=n_{H\left(NH_4NO_3\right)}+n_{H\left(H_2O\right)}\)
=> 3,3 = 4.0,05 + 2.nH2O
=> nH2O = 1,55(mol)
Theo ĐLBTKL:
\(m_{hh\left(bd\right)}+m_{HNO_3}=m_{muoi}+m_{NH_4NO_3}+m_{NO}+m_{N_2}+m_{H_2O}\)
=> hh muỗi khan = \(m_{muoi}+m_{NH_4NO_3}=11,9+3,3.63-30.0,1-28.0,2-18.1,55=183,3\left(g\right)\)
=> A
Đặt \(n_{NO}=a(mol);n_{N_2}=b(mol)\)
\(\Rightarrow \begin{cases} a+b=\dfrac{6,72}{22,4}=0,3(mol)\\ \dfrac{30a+28b}{a+b}=2.\dfrac{43}{3}=\dfrac{86}{3} \end{cases}\Rightarrow \begin{cases} a=0,1(mol)\\ b=0,2(mol) \end{cases}\\ \Rightarrow \Sigma n_{HNO_3}=4n_{NO}+12n_{N_2}+10n_{NH_4NO_3}=3,3(mol)\\ \Rightarrow V_{dd_{HNO_3}}=\dfrac{3,3}{1}=3,3(l)\\ n_{NO_3-(muối)}=3n_{NO}+10n_{N_2}+8n_{NH_4NO_3}=2,7(mol)\\ \Rightarrow m_{muối}=m_{NO_3-(muối)}+m_{KL}+m_{NH_4NO_3}=2,7.62+11,9+0,05.80=183,3(g) \)
Chọn A