Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)
\(CH\equiv CH+H_2\underrightarrow{^{Pd,t^0}}CH_2=CH_2\)
\(nCH_2=CH_2\underrightarrow{^{t^0,p,xt}}\left(-CH_2-CH_2-\right)_n\)
\(CH_2=CH_2+H_2O\underrightarrow{^{170^0C,H^+}}C_2H_5OH\)
\(C_2H_5OH+O_2\underrightarrow{\text{men giấm}}CH_3COOH+H_2O\)
\(2CH_3COOH+Ca\left(OH\right)_2\rightarrow\left(CH_3COO\right)_2Ca+2H_2O\)
\(CaC_2 + 2H_2O \to Ca(OH)_2 + C_2H_2\\ C_2H_2 + H_2 \xrightarrow{t^o,xt} C_2H_4\\ C_2H_4 + H_2O \xrightarrow{t^o,xt} C_2H_5OH\\ C_2H_5OH + O_2 \xrightarrow{men\ giấm} CH_3COOH + H_2O\\ 2CH_3COOH + CaO \to (CH_3COO)_2Ca + H_2O\\ nCH_2=CH_2 \xrightarrow{t^o,p,xt} (-CH_2-CH_2-)_n\)

Bài 1:
- Đổ dd vào các chất rồi khuấy đều, sau đó nhúng quỳ tím
+) Tan và làm quỳ tím hóa đỏ: P2O5
+) Tan, dd vẩn đục và làm quỳ tím hóa xanh: CaO
+) Không tan: MgO
Bài 3:
PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
a_______a________a_____a (mol)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
b_______b_______b_____b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}24a+56=8\\a+b=\dfrac{4,48}{22,4}=0,2\end{matrix}\right.\) \(\Leftrightarrow a=b=0,1\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{24\cdot0,1}{8}\cdot100\%=30\%\\\%m_{Fe}=70\%\\C_{M_{H_2SO_4}}=\dfrac{0,1+0,1}{0,5}=0,4\left(M\right)\end{matrix}\right.\)

Hướng dần
- Viết hai phương trình hoá học.
- Muốn điều chế n mol CuSO 4 thì số mol H 2 SO 4 trong mỗi phản ứng sẽ là bao nhiêu ?
Từ đó rút ra, phản ứng của H 2 SO 4 với CuO sẽ tiết kiệm được H 2 SO 4
Ta có phương trình:
CuO + H 2 SO 4 → CuSO 4 + H 2 O
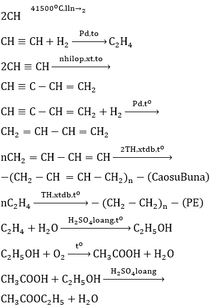
Rượu:C2H4 + H2O → C2H5OH
Axit:
- Axit axetic tác dụng với oxit bazo, bazo tạo thành muối và nước
CH3COOH + NaOH → CH3COONa + H2O
Ví dụ cho axit axetic tác dụng với natri axetat (CH3COONa), ta có phương trình:
CH3COOH + CaO → (CH3COO)Ca + H2O
- Axit axetic tác dụng với kim loại trước H giải phóng H2
2CH3COOH + 2Na → 2CH3COONa +H2
- Axit axetic tác dụng với axit yếu hơn
2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2 +H2O