Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Vì Cu không tác dụng với HCl nên ta có chất rắn không tan là Cu
\(Theo-\text{đ}\text{ề}-b\text{ài}-ta-c\text{ó}:\) nCuO = \(\dfrac{12}{80}=0,15\left(mol\right)\) ; nCu= \(\dfrac{6,6}{64}\approx0,103\left(mol\right)\)
Ta có PTHH :
CuO + H2\(-^{t0}\rightarrow Cu+H2O\)
Theo PTHH ta có :
\(nCuO=\dfrac{0,15}{1}mol>nCu=\dfrac{0,103}{1}mol\) nên => nCuO dư ; nCu hết
Ta có :
\(H=\dfrac{\left(s\text{ố}-mol-ch\text{ất}-thi\text{ếu}\right)}{\left(s\text{ố}-mol-ch\text{ất}-d\text{ư}\right)}.100\%=\dfrac{0,103}{0,15}.100\%\approx68,67\%\)
Vậy ...............

P1: Gọi số mol CO, H2 trong phần 1 là a, b mol
PTHH: CuO + CO --to--> Cu + CO2
CuO + H2 --to--> Cu + H2O
\(n_{Cu}=\dfrac{4,48}{64}=0,07\left(mol\right)\)
=> a + b = 0,07 (1)
P2: Gọi số mol CO, H2 trong phần 2 là ak, bk mol
=> 28ak + 2bk - 28a - 2b = 1,32 (2)
\(n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
PTHH: CO + O2 --to--> CO2
CO2 + Ca(OH)2 --> CaCO3 + H2O
=> ak = 0,06 (mol) (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,02\\b=0,05\\k=3\end{matrix}\right.\)
=> m = (0,02.28 + 0,05.2) + (0,06.28+0,15.2) = 2,64(g)
\(\left\{{}\begin{matrix}\%CO=\dfrac{0,02}{0,07}.100\%=28,57\%\\\%H_2=\dfrac{0,05}{0,07}.100\%=71,43\%\end{matrix}\right.\)

nCuO=0,02 mol
CuO+H2=>H2O+Cu
Bđ0,02 mol
Pứ:x mol =>x mol
Dư:0,02-x mol
Cr sau pứ gồm Cu và CuO
=>64(0,02-x)+80x=1,344
=>16x=0,064=>x=0,004
H%=0,004/0,02.100%=20%

2H(Axit) + O(Oxit) → H2O
→ nH(Axit) = 2.nO(Oxit)
Gọi số mol của Fe3O4 và CuO lần lượt là x và y
BTNT O: 4x + y = 0,6
BTKL: 56 . 3x + 64y = 29,6
=> x = 0,1 và y = 0,2
=> %Fe3O4 = 59,18%
%CuO = 40,82%

\(n_{FeO\left(bđ\right)}=a\left(mol\right);n_{CuO\left(bđ\right)}=y\left(mol\right)\\ n_{Cu}=\dfrac{0,64}{64}=0,01\left(mol\right)\)
\(\Rightarrow72a+80y=2,28\left(1\right)\)
\(PTHH:\\ FeO+H_2\underrightarrow{t^o}Fe+H_2O\\CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Vì phản 1 thời gian (phản ứng không hoàn toàn) nên sau phản ứng còn FeO, CuO dư. Vậy 1,96g hỗn hợp rắn thu được gồm Fe: x (mol); Cu: 0,01(mol); FeO dư: a - x (mol); CuO dư: y - 0,01 (mol)
Ta có phương trình:
\(56x+0,64+72\left(a-x\right)+80\left(y-0,01\right)=1,96\\ 72a+80y-16x=1,8\left(2\right)\)
\(\left(1\right)\left(2\right)\Rightarrow2,28-16x=1,8\Leftrightarrow x=0,03\left(mol\right)\)
\(\Rightarrow m=m_{Fe}+m_{Cu}=56.0,03+0,64=2,32\left(g\right)\)

CuO + CO \(\xrightarrow{t^o}\) Cu + CO2
1.......................1.........................(mol)
Fe3O4 + 4CO \(\xrightarrow{t^o}\) 3Fe + 4CO2
1.............................3......................(mol)
X : $Cu,Fe,BaO,Al_2O_3$
Y : $CO,CO_2$
BaO + H2O → Ba(OH)2
1............................1....................(mol)
Al2O3 + Ba(OH)2 → Ba(AlO2)2 + H2O
1..............1.........................................................(mol)
E :$Ba(AlO_2)_2$
Q : $Cu,Fe$
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
3............6................................6............(mol)
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
1...........2...................................2............(mol)
Fe(NO3)2 + AgNO3 → Ag + Fe(NO3)3
2....................2..............2........................(mol)
T gồm : $Cu(NO_3)_2,Fe(NO_3)_3$
F gồm : $Ag$
2CO_2 + Ba(AlO2)2 + 4H2O → 2Al(OH)3 + Ba(HCO3)2
G : $Ba(HCO_3)_2$
H : $Al(OH)_3$

Đặt \(n_{K_2O}=n_{CuO}=n_{Fe_3O_4}=n_{Al_2O_3}=1\left(mol\right)\)
=> \(n_{hh}=4\left(mol\right)\)
- Cho hỗn hợp + CO dư :
\(CO+CuO-^{t^o}\rightarrow Cu+CO_2\)
\(4CO+Fe_3O_4-^{t^o}\rightarrow3Fe+4CO_2\)
=> Khí B là CO2 (5 mol) và CO dư
A gồm K2O (1 mol) ,Al2O3 (1 mol) , Fe (3 mol), Cu (1 mol)
- Cho A + H2O dư
\(K_2O+H_2O\rightarrow2KOH\)
\(2KOH+Al_2O_3\rightarrow2KAlO_2+H_2O\)
=> Dung dịch C : KAlO2 (2 mol)
Phần không tan D : Fe (3 mol) , Cu (1 mol)
- Cho D + AgNO3
\(n_{AgNO_3}=2n_{hhbandau}=8\left(mol\right)\)
\(2AgNO_3+Fe\rightarrow2Ag+Fe\left(NO_3\right)_2\)
\(2AgNO_3+Cu\rightarrow2Ag+Cu\left(NO_3\right)_2\)
=> \(n_{AgNO_3\left(pứ\right)}=3.2+1.2=8\left(mol\right)\) => AgNO3 phản ứng hết
=>Dung dịch E gồm : Fe(NO3)2 (1 mol) , Cu(NO3)2 (1 mol)
Chất rắn F gồm : Ag (8 mol)
- Khí B : CO2 (5 mol) và CO dư sục qua dung dịch C KAlO2 (2 mol)
\(KAlO_2+CO_2+2H_2O\rightarrow Al\left(OH\right)_3+KHCO_3\)
=> Dung dịch H : KHCO3
Kết tủa I : Al(OH)3
(Làm bài này xong tui muốn tắt thở luôn =))))) Chúc em học tốt nha <3 ))
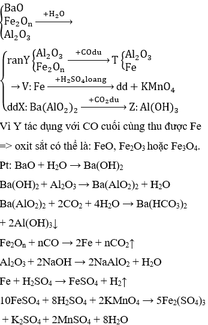
CuO + H2 to-----> Cu + H2O
0,15----> 0,15-------->0,15
nCuO=m/M=12/80= 0,15 (mol)
mCuO=M.n=64.0,15=9,6(g)
HCuO=(mcupư/mcudư).100%=(6,6/9,6).100%=68.75%