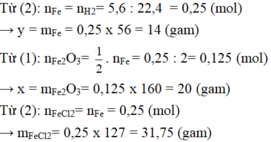Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 5:
PTHH : H2+ Cl2 -to-> 2 HCl
Vì số mol , tỉ lệ thuận theo thể tích , nên ta có:
25/1 = 25/1 => P.ứ hết, không có chất dư, tính theo chất nào cũng được
=> V(HCl)= 2. V(H2)= 2. 25= 50(l)
Câu 4: mFe2O3= 0,6. 80= 48(g)
=> nFe2O3= 48/160=0,3(mol)
mCuO= 80-48=32(g) => nCuO=32/80=0,4(mol)
PTHH: CuO + CO -to-> Cu + CO2
0,4_______0,4_____0,4____0,4(mol)
Fe2O3 + 3 CO -to-> 2 Fe +3 CO2
0,3_____0,9____0,6______0,9(mol)
=>nCO= 0,4+ 0,9= 1,3(mol)
=> V(CO, đktc)= 1,3. 22,4=29,12(l)

a/ nAl= 54/27= 2(mol)
nO2=48/32=1,5(mol)
PTHH: 2 Al2O3 -to-> 4 Al +3 O2
Ta có: 2/4 = 1,5/3
=> P.ứ hết
=> nAl2O3= 1/2. nAl=1/2. 2=1(mol)
=> mAl2O3=1.102=102(g)
b) %mAl2O3= (102/127,5).100= 80%

Phương trình hóa học của phản ứng:
Fe + H2SO4 → FeSO4 + H2.
Zn + H2SO4 → ZnSO4 + H2.
Fe + 2HCl → FeCl2 + H2.
Zn + 2HCl → ZnCl2 + H2.
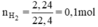
Theo phương trình (3) mFe cần dùng: 56.0,1 = 5,6g.
Theo phương trình (4) mZn cần dùng: 65.0,1 = 6,5g.

Bài 3 :
PTHH : \(6Fe+4O_2\left(t^o\right)->2Fe_3O_4\) (1)
\(n_{Fe_3O_4}=\dfrac{m}{M}=\dfrac{2,32}{56.3+16.4}=0,01\left(mol\right)\)
Từ (1) => \(3n_{Fe_3O_4}=n_{Fe}=0,03\left(mol\right)\)
=> \(m_{Fe}=n.M=1,68\left(g\right)\)
Từ (1) => \(2n_{Fe_3O_4}=n_{O_2}=0,02\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=n.22,4=0,448\left(l\right)\)
Bài 4 :
PTHH : \(4P+5O_2\left(t^o\right)->2P_2O_5\) (1)
\(n_P=\dfrac{m}{M}=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{6,72}{32}=0,21\left(mol\right)\)
Có : \(n_P< n_{O_2}\left(0,2< 0,21\right)\)
-> P hết ; O2 dư
Từ (1) -> \(\dfrac{1}{2}n_P=n_{P_2O_5}=0,1\left(mol\right)\)
=> \(m_{P_2O_5}=n.M=14,2\left(g\right)\)
Bài 3:
\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
PTHH: 3Fe + 2O2 ---to→ Fe3O4
Mol: 0,03 0,02 0,01
\(m_{Fe}=0,03.56=1,68\left(g\right);V_{O_2}=0,02.22,4=0,448\left(l\right)\)