Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

bảo toàn khối lượng ta có: 8,66+6,48+\(m_{khí}\)=28,99
--->\(m_{muối}\)=28,99-8,66-6,48=13,85g\(n_{khí}\)=5,6/22,4=0,25 molgọi a,b lần lượt là số mol của O2 và Cl2ta có: a+b=0,25 32a+71b=13,85--->a=0,1 mol;b=0,15 molta có:\(n_{Al}\)=0,12/1,5=0,08 mol\(n_{Zn}\)=0,15/1,5=0,1 mol(vì khối lượng hỗn hợp ba đầu gấp 1,5 lần khối lượng hỗn hợp lúc sau) \(Al^0\)---->\(Al^{+3}\)+3emol: 0,08--------------->0,24 \(Zn^0\)--->\(Zn^{+2}\) +2emol: 0,1-------------->0,2 \(R^0\)--->\(R^{+n}\)+ne(với n là hóa trị của R)mol: 2\(H^+\) +2e--->\(H2\)mol: 0,28 0,14 \(O2\) +4e--->2\(O^{-2}\)mol: 0,1---->0,4 \(Cl2\) +2e---->2\(Cl^-\)mol: 0,15----->0,3bảo toàn e ta có: \(\frac{6,48}{R}=\frac{0,4+0,3+0,28-0,24-0,2}{n}\)-->12n=R-->n=2--->R=24(Mg)bảo toàn khối lượng ta có: \(m_{muối}\)=28,99+0,14.2.36,5-0,14.2=38,93g
2yAl + 3FexOy ---> yAl2O3 + 3xFe (1) Chất rắn B gồm Al2O3, Fe và Al dư (vì phản ứng xảy ra hoàn toàn nên FexOy không dư).
0,08 0,04 0,08
Al(dư) + NaOH + H2O ---> NaAlO2 + 3/2H2 (2)
0,02 0,02 0,03 mol
Al2O3 + 2NaOH ---> 2NaAlO2 + H2O (3) Phần không tan D là Fe.
NaAlO2 + HCl + H2O ---> Al(OH)3\(\downarrow\)+ NaCl (4)
2Al(OH)3 ---> Al2O3 + 3H2O (5) (5,1 gam chất rắn là Al2O3).
0,1 0,05 mol
2Fe + 6H2SO4 ---> Fe2(SO4)3 + 3SO2\(\uparrow\) + 6H2O (6)
0,08 0,12 mol
Theo pt(4) và (5) số mol NaAlO2 = số mol Al(OH)3 = 0,1 mol. Do đó số mol NaAlO2 ở pt (3) = 0,1 - 0,02 = 0,08 mol. Suy ra số mol Al2O3 sinh ra ở pư (1) = 0,04 mol.
Theo pt(6) số mol Fe = 0,08 mol. Như vậy, từ pt (1) ta có: 2y = 3x hay x/y = 2/3. Suy ra: Fe2O3.
m = mAl + mFe2O3 = 27(0,08 + 0,02) + 160.0,04 = 9,1 gam.

Gọi x,y tương ứng là số mol của FeO và Fe2O3
Ta có: 72x + 160y = 78,4 và 127.x/2 + 325.y/2 = 77,7. Giải hệ thu được: x = 0,2;y = 0,4 mol.
mFeO = 72.0,2 = 14,4 gam; mFe2O3 = 78,4 - 14,4 = 64 gam.
Phần 2:
Gọi a, b tương ứng là số mol của HCl và H2SO4. Hỗn hợp muối khan gồm FeCl2, FeCl3, FeSO4 và Fe2(SO4)3.
Ta có: 83,95 = mFe + mCl + mSO4 = 56(0,1 + 0,4) + 35,5a + 96b = 28 + 35,5a + 96b
Mặt khác: nCl + 2nSO4 = a + 2b = 2nFeO + 6nFe2O3 = 2.0,1 + 6.0,2 = 1,4
Giải hệ thu được: a = 0,9 và b = 0,25 mol.
Vậy: [HCl] = 0,9/0,5 = 1,8M và [H2SO4] = 0,25/0,5 = 0,5M.

Ta có phản ứng:
X + HCl \(\rightarrow\) XCl + 1/2H2 (1)
m 36,5x 26,6 g x (g)
Dung dịch Y chứa XCl và HCl dư (có cùng nồng độ nên sẽ có cùng số mol).
Nếu gọi x là số mol của XCl thì 0,4 - x sẽ là số mol của HCl dư. Do đó: x = 0,4 - x, suy ra: x = 0,2 (mol).
Áp dụng định luật bảo toàn khối lượng cho phương trình (1), thu được: m + 36,5x = 26,6 + x. Như vậy: m = 19,5 (g).
2X + Cl2 \(\rightarrow\) 2XCl (2)
m 0,1.71 m1 (g)
m1 = m + 7,1 = 26,6 (g).

Đáp án : B
Xét P1 và P2 : khi số mol HCl tăng thì khối lượng rắn tăng => ở P1 HCl thiếu
=> mrắn – mP1 = mCl pứ => nCl pứ = 0,5 mol = nHCl = 0,5a
=> a = 1 M
Gọi số mol Zn , Mg , Fe trong mỗi phần lần lượt là x , y , z
+) P2 : mrắn – mP2 = mCl pứ => nCl pứ = 0,7 mol < nHCl => kim loại phản ứng hết
=> 2x + 2y + 2z = 0,7 mol
+) P3 : nAg = 2nZn + 2nMg + nFe => 2x + 2y + 3z = 0,8 mol
,mmỗi P = 65x + 24y + 56z = 15,7g
=> x = z = 0,1 ; y = 0,15 mol
=> %nMg = 42,86%

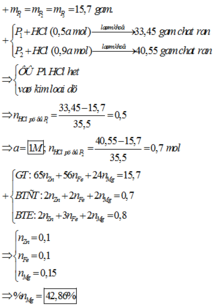


câu 1. giải hệ phương trình: \(\begin{cases}27x+65y=6,05\\133,5x+136y=13,15\end{cases}\)=>\(\begin{cases}x=\frac{3}{470}\\y=\frac{17}{188}\end{cases}\)=> nHCL= 3.(3/470)+2.(17/188)=0,2(MOL)
==> mct= 7,3 (g)
ta có C%=(mct/mdd).100%===> mdd=73(g)
câu 2.
từ ct trên===> mct của AgN03=17(g)===> nAgN03=0,1(mo)====> CM HCl= n/V=2/3(M)
câu 3.
ta có Al+ 3HCl===> AlCl3+ 3/2H2
0.2(mol)======> 3/2. 0,2=0.3( mol)
=====> v H2= 0,3. 22,4=6,72(l)